Revisión
La terapia con células madre en la degeneración del epitelio pigmentario de la retina
Stem cell therapy in degeneration of the retinal pigment epithelium
Actual. Med. 2015; 100: (795): 88-93 DOI: 10.15568/am.2015.795.re01
Enviado:10-03-2015
Revisado:14-08-2015
Aceptado: 21-08-2015
RESUMEN
Las enfermedades retinianas constituyen un grupo de patologías de gran impacto en la sociedad actual. Algunas entidades, como la degeneración macular asociada a la edad (DMAE), primera causa actual de ceguera en el mundo occidental, la enfermedad de Stargardt y la retinitis pigmentaria, comparten una alteración histológica común, la degeneración del epitelio pigmentario de la retina (EPR). Actualmente, no existe tratamiento para todas ellas, y las opciones terapéuticas de las que disponemos, no siempre son efectivas o no llegan a producir la completa recuperación, además de suponer una gran carga asistencial y un elevado coste. Ante esta situación surge la necesidad de investigar sobre la terapia con células madre para lograr la restauración o sustitución del EPR. Las células madre se presentan como una alternativa terapéutica para estos pacientes, que está mostrando resultados prometedores. En este trabajo se realiza, en primer lugar un resumen sobre las generalidades de estas patologías, para después hacer un recorrido por la trayectoria de la terapia celular en la patología retiniana en los últimos años. Se describen los hallazgos principales en cuanto a diferentes tipos celulares: células madre embrionarias, fetales, de cordón umbilical y hematopoyéticas y mesenquimales procedentes de médula ósea. Se comentan además algunas de las investigaciones y ensayos clínicos más significativos que se están llevando a cabo actualmente alrededor de todo el mundo.
ABSTRACT
Retinal diseases are a group of diseases with great impact in today´s society. Some entities, such as age-related macular degeneration (AMD), first current cause of blindness in the western world, Stargardt´s disease and retinitis pigmentosa, share a common histological alteration, degeneration of the retinal pigment epithelium (RPE). Currently, there is not treatment for all of them, and treatment options that are available not always achieve healing or not produce the complete recovery, representing a large healthcare burden and high cost. This situation arises the need for research on stem cell therapy to achieve the restoration or replacement of the RPE. Stem cells are presented as a therapeutic alternative for these patients, that is showing promising results. In this work, firstly we do a summary about the general characteristics of these pathologies, and subsequently we do a journey through the path of cell therapy in retinal pathology in recent years. We describe the main findings about some different cell types: embryonic, foetal, from umbilical cord and bone marrow derived hematopoietic and mesenchymal stem cells. Also we discusse some of current investigations and major trials that are being conducted at present round the world
Leer Artículo Completo
INTRODUCCIÓN
Actualmente existe un gran número de pacientes afectos por patologías retinianas, tanto de forma adquirida en edades por encima de los 50 años generalmente, como de manera congénita en niños y jóvenes, que causan un gran impacto sobre su calidad de vida. Los tratamientos de los que disponemos para estas enfermedades, en algunos casos no son efectivos, o no llegan a producir una completa recuperación. Esto ocurre en algunas entidades patogénicas tales como, la degeneración macular asociada a la edad, primera causa de ceguera legal en Europa, con una afectación mundial aproximada de 30 millones de personas (1,2).
Ante las escasas posibilidades terapéuticas o su baja tasa de éxito en determinadas enfermedades retinianas, surge la necesidad de investigar otras vías de tratamiento, como la terapia celular con células madre. Sin embargo, la anatomía y fisiología de la retina es compleja, ya que se encuentra formada por numerosas capas que mantienen una interrelación estrecha para lograr su completo funcionamiento; por ello las primeras investigaciones basadas en células madre se han dirigido hacia la sustitución o reparación de una única capa celular. De esta forma, las primeras patologías susceptibles de ser tratadas podrían ser aquellas cuyo daño principal se encuentra localizado en una sola capa retiniana, como las enfermedades del epitelio pigmentario de la retina (EPR). Entre las patologías sobre las que se está estudiando actualmente el potencial beneficio de la reparación o sustitución del epitelio pigmentario se encuentran principalmente: la degeneración macular asociada a la edad (DMAE), la Enfermedad de Stargardt y la Retinitis Pigmentaria.
El epitelio pigmentario de la retina es una monocapa epitelial polarizada, derivada de la placa neural anterior, cuyos límites anatómicos son los segmentos externos de los fotorreceptores, en su cara interna, y la membrana de Bruch en su porción externa. Entre sus funciones principales, están las de soporte, reciclaje del retinol, fagocitosis de los segmentos externos de conos y bastones y la producción de factores de crecimiento (3). Inicialmente, se comenzó estudiando la sustitución del EPR con células autólogas, y progresivamente se han ido ampliando las investigaciones en torno a la terapia con células madre, y células madre pluripotentes inducidas (iPSCs), tanto para reemplazo como para regeneración tisular, mediante distintos modelos de utilización, como la inyección de suspensiones celulares o el injerto de monocapas cultivadas mediante técnicas de Ingeniería Tisular.
En este trabajo, se realiza un recorrido por los hallazgos más significativos de la terapia celular con células madre en las patologías que afectan al EPR, sus posibles aplicaciones, potenciales ventajas y limitaciones, las principales líneas de investigación y ensayos clínicos que se están siguiendo en la actualidad, así como las perspectivas futuras de este tipo de terapias.
CUERPO DE REVISIÓN
1. GENERALIDADES SOBRE EL EPR Y SUS ALTERACIONES
El EPR es una monocapa celular polarizada, con origen embriológico en la placa neural anterior, que posee una gran actividad metabólica imprescindible para el circuito visual. En su porción apical, el EPR se encuentra enfrentado con los segmentos externos de los fotorreceptores, con los que mantiene una estrecha relación por medio de sus microvellosidades. En su porción basal, limita con la membrana de Bruch, que lo mantiene separado del endotelio de la capa coriocapilar. Cada célula del EPR se encuentra estrechamente unida a sus células contiguas, fomando la barrera hemato-retiniana externa, y a su vez, cada célula se adhiere a la membrana de Bruch. En el citoplasma de las células del EPR, desplazado hacia su polo apical, encontramos como estructuras principales, un núcleo celular dezplazado hacia el polo basal y numerosos gránulos de melanina (3).
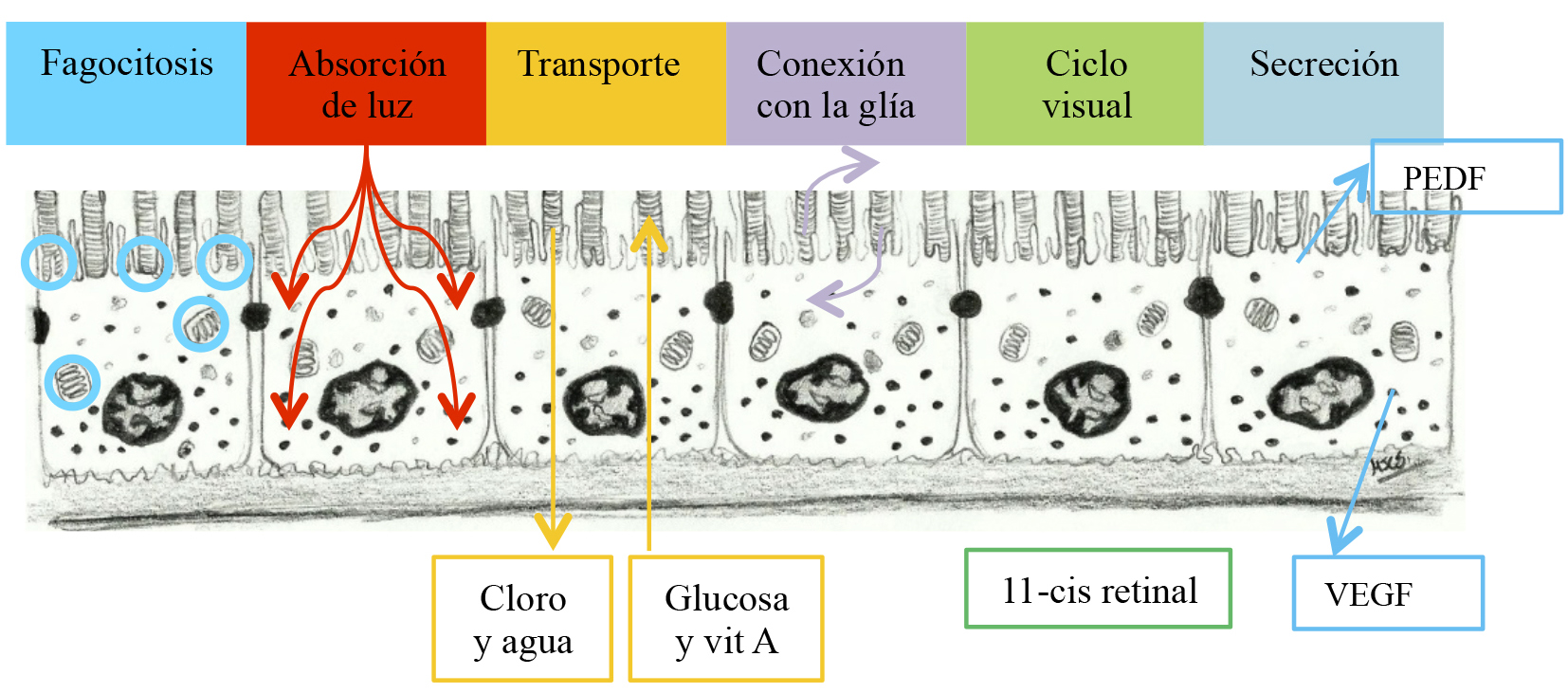
Entre las funciones principales del EPR, se encuentran el transporte de nutrientes hacia los fotorreceptores, así como de productos metabólicos finales a la sangre. Se encuentra implicado en la absorción de luz y el ciclo del retinol, permitiendo el mantenimiento del estado de excitabilidad de los fotorreceptores mediante la conversión de las formas trans en cis-retinal. Por otra parte, se encargan de la fagocitosis de los segmentos externos de los fotorreceptores, y de la secreción de factores de crecimiento como el factor de crecimiento del endotelio vascular (VEGF) por su lado basal, y el factor derivado del epitelio pigmentario (PEDF) por su lado apical (3,4) (Figura 1).
Figura 1. Funciones principales del EPR: Fagocitosis de los segmentos externos de los fotorreceptores, absorción de luz, transporte de nutrientes hacia los fotorreceptores y de productos de desecho a la sangre, ciclo del retinol, segregación basal de factor de crecimiento del endotelio vascular (VEGF), y apical de factor derivado del epitelio pigmentario (PEDF).
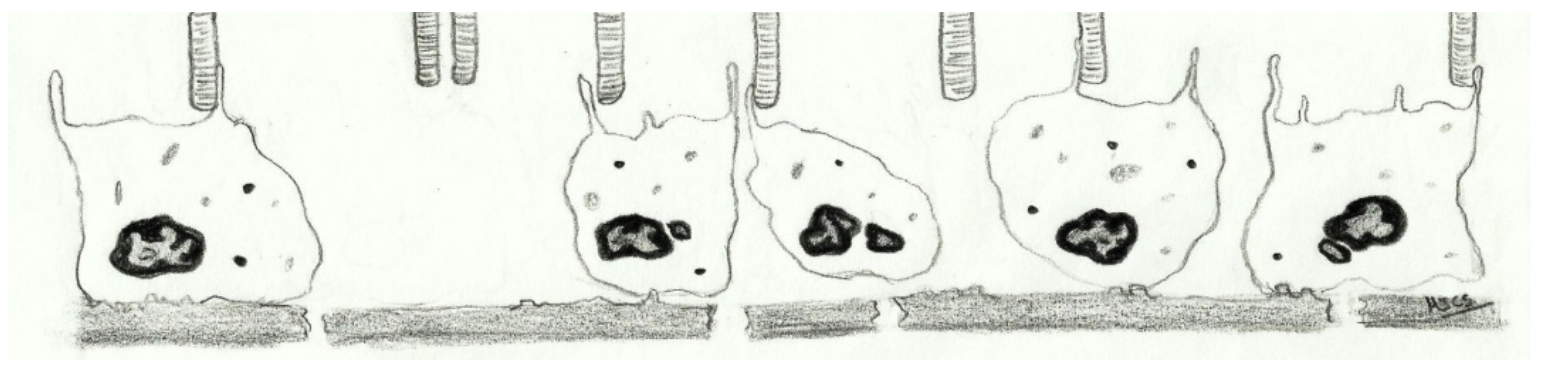
Cuando el EPR se degenera, su arquitectura normal se distorsiona, pudiendo observarse un epitelio de aspecto discontinuo con pérdida de adhesiones estrechas intercelulares y con la membrana de Bruch, así como menor relación de las microvellosidades con los segmentos externos de los fotorreceptores y disminución de su fagocitosis (3) (Figuras 2 y 3).
Figura 2. Epitelio pigmentario de la retina sano: A) Segmentos externos de los fotorreceptores. B) Células del epitelio pigmentario de la retina. C) Membrana de Bruch.
Figura 3. Degeneración del epitelio pigmentario de la retina: En esta imagen se ilustra la pérdida de uniones estrechas entre las células del EPR, la pérdida de adhesión a la membrana de Bruch y la disminución de la interacción EPR-segmentos externos de los fotorreceptores. También se observa una disminución de la densidad de fagosomas y gránulos en el citoplasma de las células del EPR, así como disminución en el número de fotorreceptores y discontinuidad en el espesor de la membrana de Bruch.
Existen diversas entidades patológicas, que a lo largo de su evolución van experimentando un notable deterioro en la funcionalidad del EPR, y en estadios avanzados, también de la capa de fotorreceptores. La DMAE, la enfermedad de Stargardt y la retinitis pigmentaria, se han propuesto como modelos patológicos susceptibles de tratamiento mediante la reparación o sustitución del EPR mediante células madre. A continuación se definen algunos de los rasgos más identificativos sobre ellas.
1.1 Degeneración macular asociada a la edad (DMAE):
La degeneración macular asociada a la edad (DMAE) es actualmente la primera causa de pérdida visual y ceguera legal en edades avanzadas (5). Aproximadamente el 30 % de los adultos mayores de 75 años, muestran signos de maculopatía (6). En su proceso fisiopatológico se encuentran implicados factores, de carácter genético y ambiental, que conducen a una degeneración progresiva del EPR, con acumulación de lipofucsina, y de la membrana de Bruch, que duplica su espesor habitual (6,7).
Existen dos variantes patogénicas, la DMAE seca, y la húmeda, caracterizada por la aparición de neovascularización coroidea. Para la forma seca o atrófica, no existe tratamiento actualmente, más que la prevención y la administración de complejos vitamínicos y antioxidantes. Sin embargo, la variante húmeda o exudativa, sí es susceptible de tratamiento, siendo la terapia estándar actual la inyección intravítrea de agentes anti-VEGF o la terapia combinada (terapia fotodinámica y/o anti-VEGF y/o corticoides) para los casos no respondedores (8).
La carga psicológica y económica de la DMAE es importante, y a menudo, poco reconocida. Los pacientes con DMAE refieren cierta angustia visual que se refleja en sus tareas ordinarias y repercute en el empeoramiento de su calidad de vida. Por otro lado, el tratamiento con inyecciones intravítreas de fármacos anti-VEGF y la necesidad de su aplicación por largos períodos de tiempo, conllevan un alto coste para los sistemas sanitarios, de difícil soporte en la actualidad (9).
1.2 Enfermedad de Stargardt:
La enfermedad de Stargardt es una entidad patológica de carácter hereditario, que supone la primera causa de afectación macular en niños. Se presenta entre la primera y segunda década de la vida, con una incidencia de 1:10000 nacidos vivos. Se caracteriza por la acumulación de depósitos de lipofucsina en los fotorreceptores y el EPR, que se muestran como depósitos amarillentos maculares, y que provocan gran deterioro de la visión central y atrofia del EPR (10).
La variante más común es la llamada STGD1, en la que se encuentra implicado el gen ABCA4, de herencia autosómica recesiva. Actualmente, no existen tratamientos aprobados para esta enfermedad (11).
1.3 Retinitis pigmentaria:
La retinitis pigmentaria engloba un grupo heterogéneo de degeneraciones retinianas hereditarias, caracterizadas por disfunción progresiva de los fotorreceptores y otras capas retinianas, como el EPR. Esta enfermedad constituye la primera causa de ceguera hereditaria, afectando alrededor de un millón y medio de personas a nivel mundial, con una prevalencia de 1:4000 individuos (12, 13).
Se han identificado al menos 45 genes implicados en la retinitis pigmentaria, con patrones de herencia autosómica dominante, recesiva o ligada al cromosoma X. Las mutaciones en el gen de la rodopsina suponen aproximadamente el 30% de los casos de retinitis pigmentaria autosómica dominante. Se caracteriza por el depósito de pigmento en la periferia retiniana, y su sintomatología típica es la ceguera nocturna, con pérdida del campo visual periférico, y en fases avanzadas, afectación de la visión central. En la actualidad, no posee ningún tratamiento curativo (13).
2. TERAPIA CON CÉLULAS MADRE
Las células madre poseen las capacidades de autorrenovación y diferenciación en distintos tipos celulares. En este trabajo se recogen los principales resultados de diferentes investigaciones a partir de los siguientes tipos celulares:
Células madre embrionarias, procedentes de la masa celular del blastocisto embrionario, con capacidad pluripotencial (14).
Células madre fetales, con capacidad multipotencial.
Células madre adultas hematopoyéticas y mesenquimales, ambas con capacidad multipotencial.
Células madre del cordón umbilical, con capacidad multipotencial (15,16).
Los primeros estudios de reemplazo de estructuras retinianas se basaron en técnicas como la traslocación de la mácula a la retina periférica sana, los injertos submaculares de EPR de zonas retinianas sanas, o la administración de suspensiones celulares de EPR periférico (17, 18). Se observaron algunas limitaciones como la escasez de muestra tisular autóloga suficiente para repoblar al completo la región macular, o en el caso de las suspensiones celulares, su escasa capacidad de adhesión a la membrana de Bruch, la organización celular en forma de rosetas, en lugar de en monocapa, y la presencia de fenómenos de apoptosis (16, 19).
La terapia con células madre, se presentó como una alternativa sin los inconvenientes citados, y que podía beneficiarse de dos líneas de tratamiento: la de reemplazo celular mediante el cultivo de estructuras celulares in vitro, para su posterior implantación en el paciente, o la de regeneración celular a través de los efectos paracrinos, por la segregación de factores tróficos en el tejido hospedador (16).
2.1 Biomateriales: generalidades
Un reto importante en la terapia celular es conseguir la firme adhesión celular a las estructuras subyacentes, como la lámina basal del EPR o la membrana de Bruch, para lograr una óptima viabilidad celular. Sin embargo, son numerosas entidades las que terminan afectando a ambas estructuras, por lo que surge la necesidad de obtener soportes artificiales con materiales biocompatibles que garanticen la buena implantación del injerto, su actividad celular y su viabilidad.
Los más empleados en terapéutica retiniana son los materiales poliméricos, siendo el más utilizado el colágeno, por la similitud con el tejido huésped en cuanto a sus propiedades mecánicas y adaptabilidad. Algunos estudios han conseguido cultivar células del EPR sobre membranas ultrafinas de colágeno, para su posterior implantación en el tejido subretiniano (20). Recientemente, otros estudios han investigado la adhesión celular a la capa colágena interna modificada, de membrana de Bruch autóloga (21).
2.2 Principales hallazgos de la terapia con células madre
2.2.1 Células madre embrionarias
Los estudios con células madre de origen embrionario han seguido principalmente dos líneas de propagación celular: espontánea o dirigida.
El método de propagación espontánea ha sido llevado a cabo mediante el cultivo de cuerpos embrioides en medio de diferenciación neuronal (22), o mediante la técnica de retirada del factor de crecimiento fibroblástico (FGF) del medio de cultivo (16, 19). El método de propagación dirigida, que resulta más rápido, aunque más laborioso y costoso que el primero, se basa principalmente en las técnicas de bloqueo de las vías de señalización Wnt y vías de señalización nodal, o en los métodos de incubación secuencial con nicotinamida y activina A (16, 23).
Los primeros modelos de regeneración del EPR in vitro con células madre embrionarias fueron prometedores, ya que las estructuras obtenidas mostraban gran similitud con el modelo humano. Se consiguió la formación de monocapas de células hexagonales, con microvellosidades apicales y melanosomas, con polaridad y orientación Na/K ATPasa apical. Mediante técnicas de análisis genético y proteico, se objetivó la expresión de proteínas implicadas en el ciclo del retinol, como RPE65, específica del EPR, así como ZO1, proteína de las uniones estrechas intercelulares, y la secreción de PEDF por la superficie apical celular (16,19).
En los modelos in vivo en rata RCS (con la mutación genética MERTK, responsable de alteraciones en la fagocitosis de los segmentos externos de los fotorreceptores en el EPR), se consiguieron muestras de funcionalidad del EPR tras la implantación de las células cultivadas en el espacio subretiniano. Vugler e Idelson, entre otros, describieron en dichos tejidos fenómenos de actividad eléctrica y fagocitosis que permitieron el retraso de la degeneración del EPR y la mejora del rendimiento visual. En ningún caso se observaron procesos infecciosos ni displásicos (19, 23).
La Universidad de California ha llevado a cabo dos estudios prospectivos en fase I/II que evalúa la seguridad, tolerabilidad y mejoría visual de nueve pacientes con enfermedad de Stargardt y nueve con DMAE atófica sometidos a trasplante subretiniano de EPR derivado de células madre embrionarias humanas. No se mostró evidencia de rechazos, proliferaciones adversas ni otros problemas de seguridad, tan solo los asociados a la cirugía vitreorretiniana y la inmunosupresión. La mejor agudeza visual corregida mejoró en diez ojos, se mantuvo estable o con ligera mejoría en siete ojos y tan sólo empeoró en un ojo. Los pacientes también refirieron mediante escalas de puntuación una sustancial mejoría de su calidad visual general, periférica, cercana y lejana. (24).
2.2.2 Células madre fetales
Las células madre fetales humanas empleadas en gran cantidad de estudios, tienen su procedencia en el tejido cerebral fetal de entre 16 y 20 semanas de gestación, de abortos fetales donados a la investigación científica. Tras el aislamiento y cultivo de las células madre fetales, estas fueron administradas mediante inyección en el espacio subretiniano.
Los estudios llevados a cabo en ratas RCS, evidenciaron la capacidad de estas células para migrar en la retina. Se observó la óptima viabilidad de las células administradas, con una mejoría en determinados parámetros histológicos y visuales. Sin embargo, la morfología adaptada y la expresión de marcadores no siguió ningún patrón definido similar al del tejido retiniano (16, 25).
Actualmente, se está estudiando el comportamiento de este tipo celular en humanos con disfunciones del EPR. La organización Retina Foundation of the Southwest (Dallas, Estados Unidos), en colaboración con las células desarrolladas por Stem Cells Inc. (Newark, Estados Unidos), han iniciado un ensayo clínico en 16 pacientes con DMAE seca (16).
Por otro lado, se está estudiando la capacidad de este tipo celular no sólo para la regeneración del EPR, sino para la regeneración y sustitución de los fotorreceptores dañados a consecuencia de una disfunción prolongada de sus estructuras subyacentes. Se han realizado estudios mediante la infusión de células madre embrionarias en el espacio subretiniano (16), y mediante el trasplante de fotorreceptores únicos, con óptimos resultados visuales (26). Algunos estudios emplearon el trasplante de fotorreceptores artificiales obtenidos mediante el cultivo de células madre embrionarias en medio de cultivo neuronal suplementado con factores como IGF1, NOG, DKK1 (27), LEFTY o activina A. Se ha demostrado que la supervivencia y el rendimiento del trasplante de fotorreceptores únicos aumentan cuando se realiza co-cultivo y doble sustitución EPR-fotorreceptor (16, 28).
2.2.3 Células madre de tejido umbilical
Las células madre derivadas del tejido umbilical humano también han sido empleadas en distintos estudios para la regeneración del EPR. En el estudio llevado a cabo por Lund, estas células fueron aisladas mediante técnicas de digestión enzimática y posteriormente expandidas mediante cultivo celular, para ser inyectadas en el espacio subretiniano de 80 ratas RCS. Las células madre de tejido umbilical mostraron una alta secreción de factor neurotrófico, que se ha relacionado con una mayor supervivencia de los fotorreceptores. Se evidenció una reducción significativa del grado de deterioro funcional en el comportamiento visual y el electrorretinograma (29).
Actualmente se está realizando un ensayo clínico en fase I/II en el Janssen Research and Development (Philadelphia, Estados Unidos), que emplea una línea celular de células madre de tejido umbilical llamada CNTO 2476, administrada mediante un sistema de catéteres a través de esclerótica y coroides hacia el espacio subretiniano en pacientes con DMAE seca (16).
2.2.4 Células madre hematopoyéticas
Esta población celular, procedente de médula ósea, también se ha mostrado como una potencial alternativa para la regeneración del EPR. Existe evidencia en ratones, de que estas células pueden migrar desde otras zonas corporales hacia la lesión retiniana, por lo que se estudió su comportamiento en ratones con lesiones retinianas inducidas. Se les inyectaron células madre hematopoyéticas alogénicas por vía intravenosa, y se observó que eran capaces de migrar hacia la lesión, proliferar y expresar marcadores específicos como el RPE65 (30, 31).
En Brasil se están realizando diversos ensayos en fases I y II sobre su aplicación mediante inyección intravítrea en la retinitis pigmentaria, las distrofias de fotorreceptores, la DMAE seca y el edema macular isquémico, con buenos resultados iniciales. En el estudio realizado sobre 5 pacientes con retinitis pigmentaria y distrofias de los fotorreceptores, la técnica se mostró como un procedimiento seguro, que consiguió mejorar la agudeza visual en 4 pacientes (32, 33).
2.2.5 Células madre mesenquimales
Existen diversos estudios sobre las células madre mesenquimales procedentes de médula ósea alogénica, mediante inyección subretiniana en ratones y ratas RCS. En ratones, se evidenció una restauración parcial de la morfología del EPR y los fotorreceptores. En ratas RCS, este tipo celular se mostró especialmente poco inmunógeno, y logró revertir el proceso de deterioro de los parámetros visuales básicos (16).
3. APLICACIONES ACTUALES DE LA TERAPIA CON CÉLULAS MADRE
Conociendo las grandes ventajas y potencial regenerativo de los tipos celulares sobre los que hemos tratado, y conociendo también sus principales limitaciones, se abre la posibilidad de investigación de las numerosas combinaciones posibles entre tipos celulares, procedimientos empleados y el uso de distintos biomateriales. A continuación, tratamos alguna de las estrategias y líneas de investigación actuales que combinan dichos conocimientos.
3.1 Adaptación de técnicas según la fase de la enfermedad (DMAE)
Algunos autores sugieren que no existe la técnica ideal para todos los pacientes, ni para todas las fases patogénicas de una misma enfermedad, sino que debe ser adaptada a las necesidades específicas del tejido. De este modo, poniendo como ejemplo la DMAE de tipo neovascular, se propone una distribución de técnicas según las alteraciones tisulares principales, clasificadas en 3 fases:
- Fase 1: Ausencia de daño, o daño en fase reversible de las células fotorreceptoras y del EPR. Técnica: Trasplante autólogo de células de EPR modificadas genéticamente para una mayor producción de PEDF, que actúen como inhibidores de VEGF. Para la modificación genética se ha sugerido el sistema de transposones Sleeping Beauty (SB100X).
- Fase 2: Degeneración irreversible de las células del EPR, pero no de los fotorreceptores. Técnica: Trasplante de células del EPR autólogas con una alta producción de PEDF, en estructura de monocapa sobre un sustrato biocompatible.
- Fase 3: Degeneración irreversible de las células del EPR y fotorreceptores. Técnica: Fabricación de una estructura tridimensional compuesta por un sustrato biocompatible sobre el que se pueda apoyar una monocapa celular creada a partir de células del EPR autólogas, y a su vez, sobre esta, se pueda cubrir con células precursoras de fotorreceptores. Se ha sugerido el uso de células madre pluripotenciales inducidas (iPSCs) para la creación de las células precursoras de los fotorreceptores (9).
3.2 Células madre pluripotenciales inducidas (iPSCs)
Las células somáticas diferenciadas pueden ser sometidas a técnicas de reprogramación genética para que adopten las propiedades de una célula madre pluripotencial. Estas células se derivan de la expresión de cuatro factores de transcripción, Oct4 y Sox2 (constantes para diversos autores) junto a Nanog y Lin28 o cMyc y Klf4 (algunos autores prefieren sustituir el protooncogen Myc por otros factores).
Estas células han sido capaces de diferenciarse espontáneamente en células del EPR, con potencial similar al de las células madre embrionarias humanas y el EPR fetal humano. A partir de iPSCs, se ha conseguido un EPR funcional organizado en monocapas celulares con polaridad , con capacidad de fagocitosis de los segmentos externos de los fotorreceptores y expresión de mRNA cuantitativamente similar al de las células madre embrionarias (34).
3.3 Terapia génica:
Los avances en el conocimiento de la fisiopatología de las enfermedades retinianas, y de los genes implicados en ella han descubierto otra amplia vía terapéutica, la terapia génica. Esta vía, tanto por sí misma, como combinada con la terapia con células madre, podría poseer un gran potencial en las futuras posibilidades de tratamiento de las degeneraciones del EPR.
Existen numerosos ensayos clínicos en fase I/II, que actualmente investigan diversas patologías retinianas con afectación del EPR de origen genético, como la enfermedad de Stargardt, la retinitis pigmentaria o la amaurosis congénita de Leber.
Se están llevando a cabo tres ensayos clínicos que estudian el reemplazo del gen RPE65 en la amaurosis congénita de Leber. Los pacientes fueron tratados mediante una inyección subretiniana de adenovirus (AAV2) portador del gen RPE65 como vector. Los pacientes experimentaron mejoría en la mejor agudeza visual corregida y el campo visual, entre otros parámetros. También se están realizando estudios sobre otros genes implicados como GUCY2D en ratones y primates (35).
3.4 London Project to Cure Blindness
Un equipo de científicos del Moorfields Eye Hospital junto con el UCL Institute of Ophthalmology (Londres, Reino Unido) y el Centre for Stem Cell Biology (Universidad de Sheffield, Reino Unido), está llevando a cabo diversos estudios sobre la sustitución y/o reparación del EPR en pacientes con DMAE. Se comenzó con estudios enfocados hacia el trasplante autólogo de EPR y las técnicas de traslocación macular, sin embargo, aunque se obtuvieron buenos resultados en cuanto a la funcionalidad del EPR, eran muy numerosas las complicaciones derivadas y el proceso quirúrgico era muy complejo.
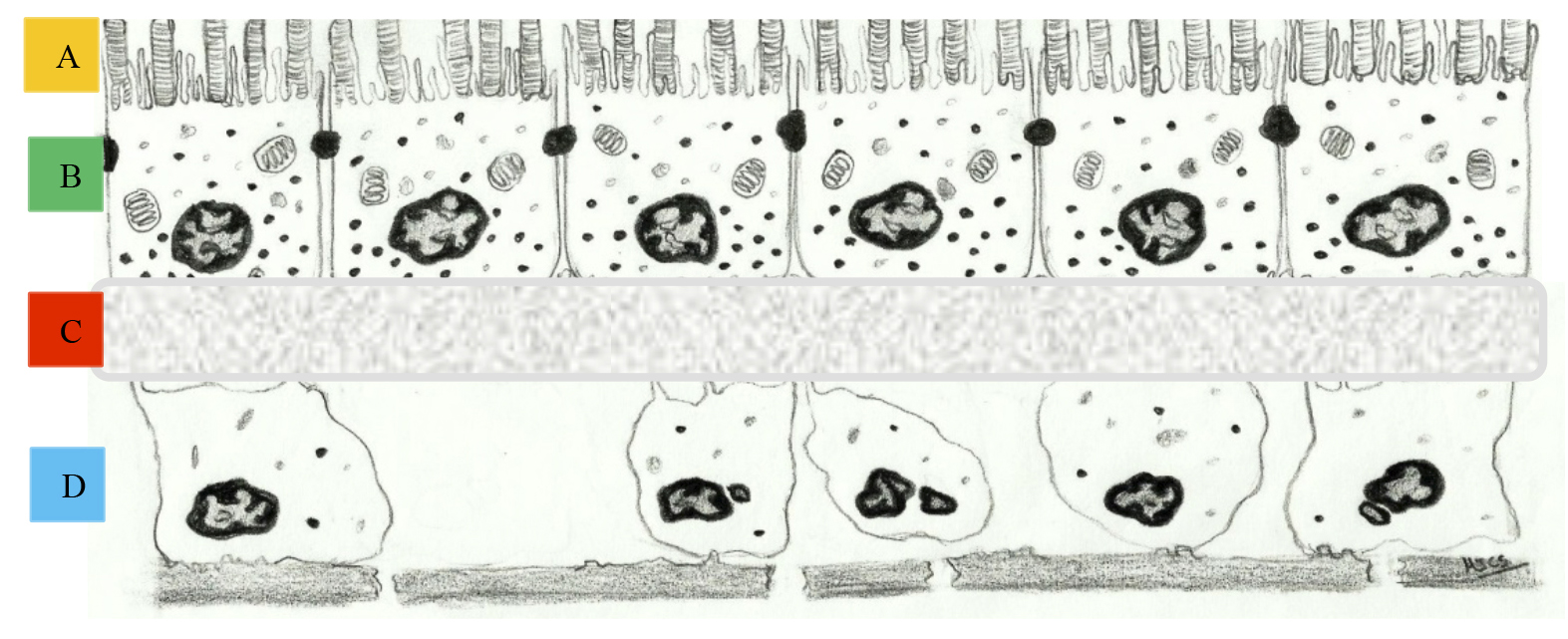
Actualmente, se está llevando a cabo un proyecto en pacientes con DMAE, basado en la implantación de una monocapa celular creada a partir de células madre cultivadas sobre una fina lámina de polímero plástico, que se apoyaría sobre el EPR dañado del paciente. De esta manera se superaría el inconveniente de la desorganización celular de las técnicas de inyección de suspensiones celulares y se garantiza una buena adhesión intercelular, una consistente estructura de soporte como sustituto de la membrana de Bruch, y una mayor facilidad para el acto quirúrgico de implantación (Figura 4).
Figura 4. Modelo propuesto: A) Segmentos externos de los fotorreceptores del paciente. B) Monocapa celular de EPR cultivada. C) Polímero plástico. D) EPR y membrana de Bruch degenerados. El modelo compuesto por la monocapa celular, cultivada sobre la fina lámina de polímero plástico, es trasplantado entre los fotorreceptores del paciente y su EPR y membrana de Bruch dañados. (16, 34, 35).
En la fase I del proyecto se desarrolló con éxito el modelo de terapia con células madre embrionarias tanto in vitro como in vivo. En fases posteriores, se pretende analizar el modelo de trasplante a partir de iPSCs, en lugar de células embrionarias, así como evaluar su capacidad de transformación en células fotorreceptoras, para su posterior implantación en los pacientes (16, 36, 37).
CONCLUSIONES
La terapia con células madre en el tratamiento de las degeneraciones del EPR ya se está aplicando en diversos ensayos clínicos, cuyos primeros resultados están siendo prometedores. Será necesario esperar a la finalización de los mismos, para lograr una mayor caracterización de los tipos celulares, perfeccionamiento de las técnicas y predecir con exactitud su comportamiento en humanos.
El próximo objetivo sería identificar la técnica de mayor efectividad en la regeneración o sustitución del EPR, con una óptima viabilidad y funcionalidad celular, mediante procesos que sean fácilmente reproducibles y seguros para el paciente.
Las técnicas basadas en iPSCs se muestran como otra posibilidad terapéutica que es capaz de sortear las dificultades éticas derivadas de otros tipos celulares como las células madre de procedencia embrionaria o el problema de escasez de fuentes de obtención celulares.
La terapia con células madre ha abierto una nueva puerta para el tratamiento de la degeneración del EPR, implicado en numerosas patologías retinianas, para algunas de las cuales no existía ninguna posibilidad terapéutica.
REFERENCIAS
- Jonas JB. Global prevalence of age-related macular degeneration. Lancet Glob Health. 2014; 2 (2): e65-6.
- Klein R, Klein B, Jensen SC, Cruickshanks KJ. The relationship of ocular factors to the incidence and progression of age-related maculopathy. Arch Ophthalmol. 1998; 116(4):506–513.
- Strauss O. The retinal pigment epithelium in visual function. Physiol. Rev. 2005; 85: 845-881.
- Strauss O. Die Rolle des retinalen Pigmentepithels im Rahmen visueller Funktionen. Der Ophthalmologe. 2009; 106: 299-304
- Klein R, Peto T, Bird A, Vannewkirk MR. The epidemiology of age-related macular degeneration. Am J Ophthalmol. 2004; 137:486–95.
- Haddad S, Chen CA, Santangelo SL, Seddon JM. The genetics of age-related macular degeneration: a review of progress to date. Surv Ophthalmol. 2006; 51:316-63.
- Zarbin MA. Current concepts in the pathogenesis of age related macular degeneration. Arch Ophthalmol. 2004; 122:598-614.
- Nowak JZ. Age-related macular degeneration (AMD): pathogenesis and therapy. Pharmacol Rep. 2006; 58 (3): 353-63.
- Fernández-Robredo P, Sancho A, Johnen S, et al. Current Treatment Limitations in Age-Related Macular Degeneration and Future Approaches Based on Cell Therapy and Tissue Engineering. J Ophtalmol. 2014; 2014:510285.
- Walia S, Fishman GA. Natural history of phenotypic changes in Stargardt macular dystrophy. Ophthalmic Genet. 2009; 30: 63-68.
- Ritter M, Zotter S, Schmidt WM, et al. Characterization of stargardt disease using polarization-sensitive optical coherence tomography and fundus autofluorescence imaging. Invest Ophthalmol Vis Sci. 2013; 54 (9): 6416-25.
- Blanco MJ, Capeans C. Retinitis pigmentaria. Med Clin. 2001; 117:135-6.
- Hamel C. Retinitis pigmentosa. Orphanet J Rare Dis. 2006; 1:40.
- Reubinoff BE, Pera MF, Fong C, et al. Embryonic stem cell lines from human blastocysts: somatic differentiation in vitro. Nat. Biotechnol. 2000; 18: 399 – 404.
- Bharti K, Rao M, Hull SC, et al. Developing cellular therapies for retinal degenerative diseases. Invest Ophthalmol Vis Sci. 2014; 55 (2): 1191-202.
- Ramsden CM, Powner MB, Carr AJ, Smart M, da Cruz L, Coffery PJ. Stem cells in retinal regeneration: past, present and future. Development. 2013; 140: 2576-2585.
- Binder S, Krebs I, Hilgers RD, et al. Outcome of transplantation of autologous retinal pigment epithelium in age-related macular degeneration: a prospective trial. Invest Ophtalmol Vis Sci. 2004; 45 (11): 4151-60.
- Chen FK., Patel PJ, Uppal GS, Tufail A, Coffey PJ, da Cruz L. Long-term outcomes following full macular translocation surgery in neovascular age-related macular degeneration. Br J Ophthalmol. 2010; 94 (10): 1337-1343.
- Vugler A, Carr A.-J, Lawrence J, et al. Elucidating the phenomenon of HESC-derived RPE: anatomy of cell genesis, expansion and retinal transplantation. Exp Neurol. 2008; 214: 347-361.
- Thumann G, Viethen A, Gaebler A, et al. The in vitro and in vivo behaviour of retinal pigment epitelial cells culture don ultrathin collagen membranes. Biomaterials. 2009; 30: 287-294.
- Sistiabudi R, Paderi J, Panitch A, Ivanisevic A. Modification of native collagen with cell-adhesive peptide to promote RPE cell attachment on Bruch’s membrane. Biotechnol Bioeng. 2009; 102(6):1723–1729.
- Meyer JS, Shearer RL, Capowski EE, et al. Modeling early retinal development with human embryonic and induced pluripotent stem cells. Proc Natl Acad Sci. 2009; 106: 16698-16703.
- Idelson M, Alper R, Obolensky A, et al. Directed differentiation of human embryonic stem cells into functional retinal pigment epithelium cells. Cell Stem Cell. 2009; 5: 396-408.
- Schwartz SD, Regillo CD, Lam BL, et al. Human embryonic stem cell-derived retinal pigment epithelium in patients with age-related macular degeneration and Stargardt’s macular dystrophy: follow-up of two open-label phase 1/2 studies. Lancet. 2015; 385 (9967): 509-16.
- McGill TJ, Cottam B, Lu B, et al. Transplantation of human central nervous system stem cells – neuroprotection in retinal degeneration. Eur J Neurosci. 2012; 35: 468-477.
- MacLaren RE, Pearson RA, MacNeil A, et al. Retinal repair by transplantation of photoreceptor precursors. Nature. 2006; 444: 203-207.
- Lamba DA, Karl MO, Ware CB, Reh TA. Efficient generation of retinal progenitor cells from human embryonic stem cells. Proc Natl Acad Sci. 2006; 103: 12769-12774.
- Zhu D, Deng X, Spee C, et al. Polarized secretion of PEDF from human embryonic stem cell-derived RPE promotes retinal progenitor cell survival. Invest Ophthalmol Vis Sci. 2011; 52: 1573-1585.
- Lund RD, Wang S, Lu B, et al. Cells isolated from umbilical cord tissue rescue photoreceptors and visual functions in a rodent model of retinal disease. Stem Cells. 2007; 25: 602-611.
- Atmaca-Sonmez P, Li Y, Yamauchi Y, et al. Systemically transferred hematopoietic stem cells home to the subretinal space and express RPE-65 in a mouse model of retinal pigment epithelium damage. Exp Eye Res. 2006; 83: 1295-1302.
- Park SS, Caballero S, Bauer G, et al. Long-term effects of intravitreal injection of GMP-grade bone-marrow-derived CD34+ cells in NOD-SCID mice with acute ischemia-reperfusion injury. Invest Ophthalmol Vis Sci. 2012; 53: 986-994.
- Siqueira RC, Messias A, Voltarelli JC, Scott IU, Jorge R. Intravitreal injection of autologous bone marrow-derived mononuclear cells for hereditary retinal dystrophy: a phase I trial. Retina. 2011; 31: 1207-1214.
- Siqueira RC, Messias A, Gurgel VP, Simões B P, Scott IU, Jorge R. Improvement of ischaemic macular oedema after intravitreal injection of autologous bone marrow-derived haematopoietic stem cells. Acta Ophthalmol. 2015; 93: e174–e176.
- Buchholz DE, Hikita ST, Rowland TJ, et al. Derivation of Functional Retinal Pigmented Epithelium from Induced Pluripotent Stem Cells. Stem Cells. 2009; 27: 2427–2434.
- Chacon-Camacho OF, Zenteno JC. Review and update on the molecular basis of Leber congenital amaurosis. World J Clin Cases. 2015; 3 (2): 112-24.
- Carr AJF, Smart MJK., Ramsden CM, Powner MB, da Cruz L, Coffey P. J. Development of human embryonic stem cell therapies for age-related macular degeneration. Trends Neurosci. 2013; 36: 385-95.
- Coffey P, da Cruz L. The London Project to Cure Blindness. The Project. [citado el 1 de junio de 2014] http://www.thelondonproject.org/?q=project/about-us.
INFORMACIÓN DEL ARTÍCULO
Autora para la correspondencia: María Jesús Chaves-Samaniego. Servicio de Oftalmología. Hospital Universitario San Cecilio. Av. Doctor Olóriz, 16. 18012, Granada. E-mail: mjchavessamaniego@gmail.com – Telf. 958 02 30 00