Original
Tratamiento de la toxicidad cutánea secundaria al tratamiento radioterápico con una crema basada en sH oligopeptide-1 (epidermal growth factor-egf): un estudio piloto
Therapy of secondary cutaneous toxicity as a result of radioterapic treatment, with a sH oligopeptide-1 cream based (epidermal growth factor-egf): a pilot study
Actual. Med. 2018; 103: (804): 76-81 DOI: 10.15568/am.2018.804.or04
Enviado: 15-06-2018
Revisado: 04-07-2018
Aceptado: 10-08-2018
RESUMEN
La dermatitis aguda es muy frecuente en pacientes tratados por neoplasias de mama, cabeza, cuello y tumores cutáneos, debido a las elevadas dosis de radiación administradas, y puede afectar hasta el 95% de los pacientes. Tales efectos pueden disminuir la calidad de vida de los pacientes. El objetivo del presente estudio es valorar como medida profiláctica frente a la radiodermatitis, la eficacia de Radio Cream® de Inves Biofarm. Se reclutaron 20 pacientes que precisaban tratamiento radioterápico, con dosis entre 42,72 Gy y 70 Gy. La crema se aplicó durante todo periodo de tratamiento, 2 veces al día. Se evaluó la toxicidad de la piel mediante los criterios del National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE), que evalúan lesiones agudas por la radiación en una escala de 0 a 4. Al finalizar el tratamiento se aprecia un porcentaje del 5%, 65% y 30% para la toxicidad grado 0, 1, 2 respectivamente, sin observarse grado 3 ni 4. En el momento de finalizar el tratamiento, un 70% no presentaban prurito y el 30% grado 1. La puntuación media de los pacientes fue de 8,38 en escala de 1 a 10. Podemos estimar que la crema Radio Cream® se ha mostrado como una opción válida para la prevención de radiodermatitis. Puede impedir o retrasar la aparición de la toxicidad cutánea, contribuyendo al mantenimiento de la calidad de vida de los pacientes y permitir completar el tratamiento radioterápico a las dosis prescritas.
Palabras clave: radiodermatitis, Epidermal Growth Factor, radioterapia, Sh-Oligopéptido-1, dermatitis.
ABSTRACT
Acute dermatitis is very common in patients being treated for breast, brain, neck and skin tumours, due to the high doses of radiation administered, and it can affect up to 95% of patients.. These effects can decrease patients’ quality of lifeThe objective of this study is to evaluate the effectiveness of Radio Cream® by Inves Biofarm as a prophylactic measure against radiodermatitis. We recruited twenty patients requiring radiotherapy, with doses between 42.72 Gy and 70 Gy. The cream was applied, twice a day. Skin toxicity was evaluated by the National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE), which assess acute radiation injuries on a scale of 0 to 4. At the end of the treatment, percentages of 5%, 65% and 30% were observed for toxicity grades 0, 1, and 2 respectively; no cases of grade 3 or 4 were found. When the treatment was finished, 70% had no pruritus and 30% had grade 1. The patients’ average score was 8.38 on a scale of 1 to 10. We can consider that Radio Cream® has proved to be a valid option for preventing radiodermatitis. It can prevent or delay the appearance of cutaneous toxicity, helping to maintain patients’ quality of life and making it possible to complete the radiotherapy at the prescribed doses.
Keywords: radiodermatitis, Epidermal Growth Factor, radiotherapy, Sh-Oligopeptide-1, dermatitis.
Leer Artículo Completo
INTRODUCCIÓN
Al menos el 50% de los pacientes diagnosticados de cáncer recibirán radioterapia (RT) durante el transcurso de su enfermedad (1). La dermatitis por RT es un efecto secundario muy frecuente, tras la administración de radiaciones ionizantes y puede afectar hasta el 95% de los pacientes (2). La dermatitis aguda es muy frecuente en pacientes tratados por neoplasias de mama, cabeza y cuello y tumores cutáneos, debido a las elevadas dosis de radiación administradas (3). La pérdida de células basales comienza con dosis de 20-25 Gy y es máxima al alcanzar los 50Gy.
El eritema (enrojecimiento de la piel), es el primer signo visible y se produce en más del 90% de los pacientes. Se produce por la dilatación de los capilares de la dermis. Posteriormente puede aparecer edema, refiriendo los pacientes, una mayor hipersensibilidad y xerosis (4). Al incrementar la dosis administrada, puede desarrollarse descamación seca con deshidratación y prurito. Con dosis más elevadas de radiación (> 40 Gy.), aparece la descamación húmeda, preferentemente en las zonas de pliegues (1).
Tales efectos pueden disminuir la calidad de vida de los pacientes (5), con la posibilidad incluso de obligar a la suspensión parcial o definitiva del tratamiento, lo que conlleva la correspondiente pérdida de eficacia del mismo.
La gravedad de dichos signos y síntomas varían en función de dos tipos de factores:
Factores intrínsecos o dependientes del propio paciente, como la edad, tratamientos previos realizados, exposición solar o radiaciones UV, tabaquismo, hidratación, tamaño de la mama, estado hormonal, obesidad y factores genéticos (1).
Factores extrínsecos: dosis y fraccionamiento administrado, energía utilizada, volumen de tratamiento e incluso la época del año en que se realiza el tratamiento.
En 2013, Wong y colaboradores (6), revisaron 56 estudios fundamentados en tratamientos para prevenir o tratar la radiodermatitis. De estos, 45 ensayos clínicos abordaron la prevención de la dermatitis, 9 sus posibles tratamientos y 2 prevención y tratamiento. La mayor parte de dichos estudios no presentaban evidencias científicas suficientes para apoyar o rechazar su uso.
Podemos considerar, por tanto, que en la actualidad no existe una profilaxis estándar dermatológica única reconocida (7;8) . Se han utilizado diversos productos a base de urea, aloe vera, caléndula entre otros principios activos, para controlar la sintomatología propia de la radiodermatitis, apreciándose discretas mejorías, sin existir en el momento presente, un acuerdo firme y unánime sobre la utilización de los mismos. Existen también cremas cuya base activa está constituida por factor de crecimiento epidérmico (EFG). Los factores de crecimiento poseen características específicas para realizar sus funciones estimulantes, destacando la relativa a unión con moléculas receptoras ubicadas en la membrana plasmática de las células diana, generando señales transmitidas mediante la activación de enzimas con actividad kinasa, mediante fosforilación proteica. La activación de la expresión génica produce la transcripción específica de ciertos genes, constituyendo la respuesta celular a dicho factor de crecimiento (9;10).
El objetivo del presente estudio piloto es valorar, como medida profiláctica frente a la radiodermatitis, la eficacia de Radio Cream® de Inves Biofarm, una crema cuyo principal componente es el Sh-Oligopeptide-1 (Epidermal Growth Factor, EGF) que favorece la regeneración y proliferación de los tejidos.
MATERIAL Y MÉTODOS
1. Diseño del estudio
Ensayos clínicos de postcomercialización
2. Población
Se reclutaron, 20 pacientes diagnosticados de cáncer que precisaban tratamiento radioterápico, con dosis entre 42,72 Gy y 70 Gy (fraccionamiento 2-2, 67 – 4Gy), con características descritas en la tabla 1. Fueron excluidos los pacientes menores de 18 años. El periodo de reclutamiento fue entre noviembre 2016 hasta febrero 2017, en el Servicio de Radioterapia de la Clínica Corachán de Barcelona. Los pacientes fueron informados mediante la hoja de información al paciente y firmaron el consentimiento informado.
Tabla 1. Datos descriptivos de los pacientes
3. Crema con base de sH Oligopeptide-1 (Epidermal Growth Factor EGF)
Se comprobó la viabilidad de utilizar crema Radio Cream®, suministrada para este estudio por Laboratorios Inves Biofarm. En su composición se incluye el Sh-Oligopeptide-1 EGF, un polipéptido presente en diferentes partes del cuerpo humano, y por tanto es compatible y biodegradable, cuyo informe de seguridad está disponible por parte del laboratorio (11), que favorece la reparación dérmica, aumentando el índice de auto-regeneración. Produce, asimismo, un incremento de la proliferación de los queratinocitos de la capa córnea, de las células endoteliales y de los fibroblastos, que favorecen la reparación cutánea al aumentar la síntesis proteica y formación de los glicosaminoglicanos. Además, en la composición de Radio Cream® se incluyen elementos no carcinógenos como: Sodium hyaluronate (HS), Aqua, Cocos Nucifera Oil, Glycerin, PEG-8 Stearate, Ceteth-20, PEG-18 Castor Oil Dioleate, PEG/PPG-4/12 Dimethicone, GlycerilStearate, EDTA, BHT, Tocopherol.
Entre los mecanismos de acción del HS, consta la estimulación del proceso de cicatrización, mediante su interacción con el fibrinógeno, acelerando la formación del coágulo de fibrina inducida por la trombina. HS se une a la molécula de fibronectina y estimula la migración epitelial, donde participan los receptores celulares CD-44 migrando a la misma región, siendo éstos, los principales receptores para el HS. Por otra parte, activa la re-epitelización, regula la proliferación y la migración de los queratinocitos y fibroblastos. El aceite de coco es un reconocido reparador natural de la piel (12), así como el tocoferol (13).
La crema se aplicó en cantidad suficiente, durante todo periodo de tratamiento, desde el día de inicio hasta un mes después de finalizar la última sesión de RT, dos veces al día, en la zona de tratamiento y con control semanal más otra visita al mes después de finalizar el tratamiento radioterápico, realizando fotografías en cada visita del área tratada.
No se permitió la administración concomitante de otro tratamiento tópico en toda la zona a estudiar, y en el caso en el que fue necesario otro tratamiento tópico, se suspendería inmediatamente la administración de Radio Cream® en esa zona y el paciente quedaría ese momento, descartado para el estudio.
4. Evaluación
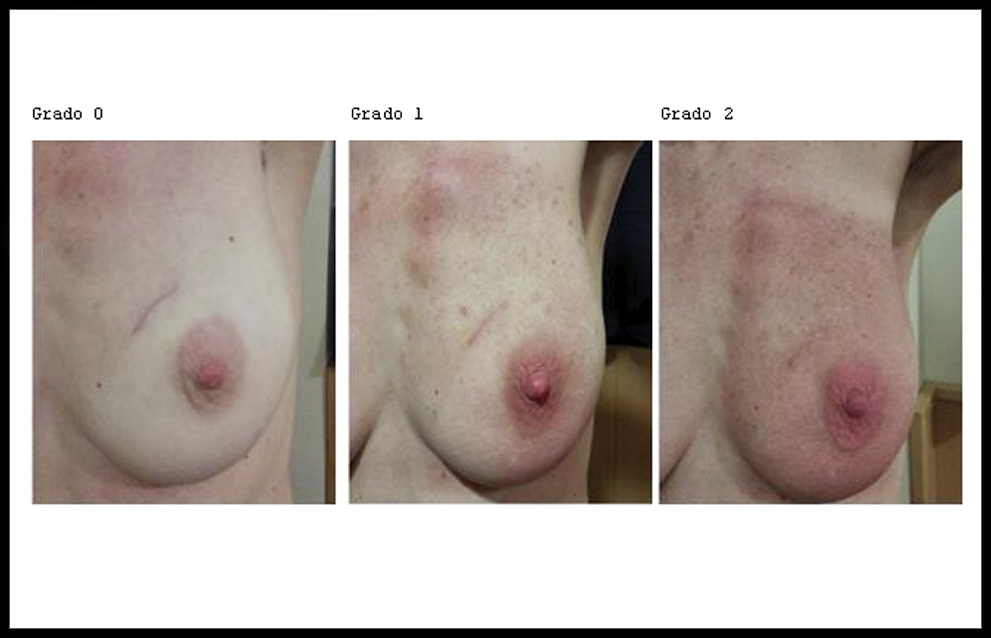
Se evaluó la toxicidad de la piel, por parte del personal médico, mediante los criterios del National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE) v3.0 (14), que evalúan lesiones agudas por la radiación en una escala de 0 a 4: Grado 0, sin reacción; Grado 1, eritema leve o descamación seca; Grado 2, eritema moderado a fuerte, descamación parcheada húmeda principalmente limitada a pliegues cutáneos, edema moderado; Grado 3, descamación húmeda no en pliegues, sangrado inducido por traumatismo menor; Grado 4, necrosis o ulceración de todo el grosor de la piel, sangrado espontáneo. El criterio de valoración primario fue el grado máximo de dermatitis por RT (Figura 1).
Figura1. Grados iniciales de toxicidades.
La eficacia de la crema Radio Cream® se evaluó comparando el estado cutáneo al inicio del tratamiento, con el momento de la administración de 50 Gy (o dosis equivalente) y nuevamente al final de la RT planificada. Otra sintomatología evaluada fue el prurito, en la zona de tratamiento.
El prurito, como síntoma que es, solo lo puede evaluar el propio paciente y se puntuó usando los criterios de la NCI CTCAE v3.0 (14): Grado 0, sin prurito; Grado 1, leve o localizado, aliviado espontáneamente; Grado 2, leve o localizado, aliviado por medidas locales; Grado 3, intenso o generalizado, aliviado por medidas sistémicas; y Grado 4, intenso o extendido y mal controlado a pesar del tratamiento.
Al finalizar el tratamiento, se realizó una breve encuesta al paciente para valorar diversos aspectos de la crema: Absorción, aroma, sensación de frescor, efectividad subjetiva, comodidad de administración y tolerabilidad, siendo la escala del 0 a 10 donde: 0 sería completamente negativo y 10 muy positivo.
RESULTADOS
1. Características del paciente y del tratamiento
Todos los pacientes (20), fueron candidatos de inicio, para evaluar la eficacia de Radio Cream® El 95% son mujeres con edad media de 60,3 años (min.40-max.77). La localización del tumor en 18 pacientes fue a nivel de glándula mamaria o pared torácica, un paciente se realizó el tratamiento a nivel de cuero cabelludo por carcinoma escamoso y otro fue tratado a nivel cervical por metástasis subcutánea secundaria a una tumoración mamaria. El 25% de los pacientes habían recibido tratamiento quimioterápico previo, incluyendo antraciclinas en sus esquemas y, dos de ellos continuaron concomitantemente el tratamiento con Trastuzumab durante la RT. La dosis media administrada fue de 60,53 Gy (42,72 Gy – 70 Gy) con un fraccionamiento de 2 – 2,67 – 4 Gy. La dosis de 42,72 Gy se administró con un fraccionamiento de 2,67 Gy, por lo que la dosis biológica equivalente sería 50 Gy o superior. La energía predominante fue mixta de fotones en toda la glándula mamaria y posterior boost con electrones en el lecho quirúrgico en 15 pacientes (75%), electrones exclusivamente en 1 paciente (5%) y fotones como única energía en 4 pacientes (20%).
Tres pacientes debieron suspender la crema al iniciar tratamiento tópico y/o sistémico con corticoides por presentar prurito no controlado con dosis de 24, 44 y 46 Gy., motivo por el cual se les excluyó de los resultados finales del estudio.
2. Grado de dermatitis
La reacción de radiación aguda generalmente aparece entre 10 y 14 días desde el comienzo de la RT, y continúa aumentando en gravedad hasta la finalización del tratamiento. La apariencia de la piel, a menudo se describe como una pérdida de células de la epidermis o peeling (descamación seca) y picazón. La reacción puede volverse más severa con diversos grados de pérdida epidérmica (descamación húmeda) y muy raramente, necrosis. La incomodidad varía de irritación leve a dolor severo (15).
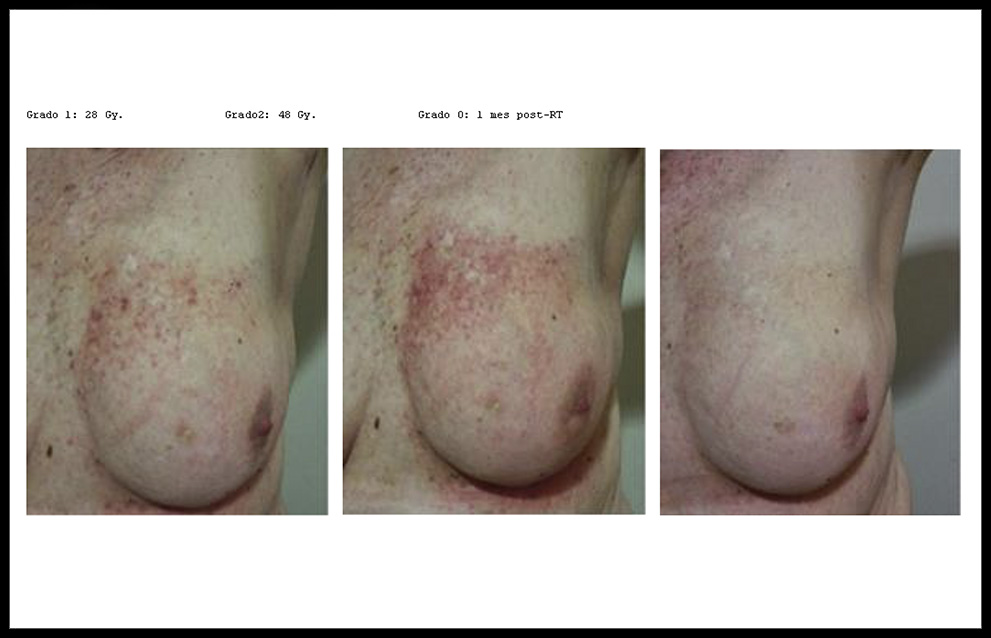
Para los 17 pacientes que se valoran, en el corte de los 50 Gy se observó una dermatitis grado 0, 1 y 2, en el 12%, 53% y 35%, respectivamente, no observándose ningún paciente con toxicidades grado 3 y 4. En este momento no se aprecian diferencias entre los pacientes que han realizado quimioterapia previa (3 pacientes grado 1 y 2 pacientes grado 2) y los que no la habían realizado (Tabla 2) y (Fig.3). En 16 pacientes (94%) se observa cualquier grado de epitelitis al finalizar el tratamiento radioterápico. Al finalizar el tratamiento se aprecia un porcentaje del 5%, 65% y 30% para la toxicidad grado 0, 1, 2 respectivamente, sin observarse grado 3 ni 4 (4 pacientes grado 1 con quimioterapia previa y 1 paciente grado 2). Se ha observado que los pacientes con mayor dermatitis eran aquellos con una mayor exposición solar previa (Fig. 2).
Figura 2. Toxicidad cutánea dibujando en cuadrantes superiores la exposición al campo de tratamiento con exposición solar previa.
3. Grado de prurito
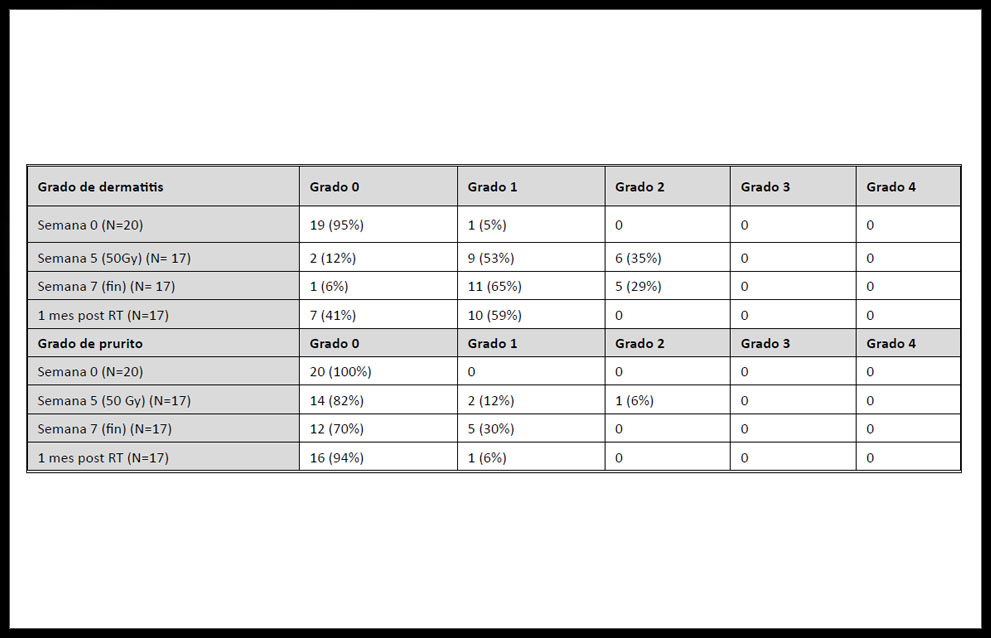
El prurito asociado al tratamiento radioterápico puede condicionar la calidad de vida del paciente oncológico. Por este motivo, se considera que la capacidad de prevenirlo mediante la administración de Radio Cream®, es fundamental para la valoración de su eficacia (Tabla 2) y (Fig.3). El grado de prurito en el momento de alcanzar la dosis de 50 Gy fue de 82%, 12%, 1%, para grado 0, 1, 2. En el momento de 50 Gy en el 25% fue eficaz Radio Cream® para prevenir o controlar dicho síntoma. En el momento de finalizar el tratamiento, un 70% no presentaban prurito y el 30% grado 1. Al mes post-tratamiento, 16 pacientes se encontraban asintomáticos y 1 paciente refería seguir presentando prurito grado 1 en la zona de sobredosis o boost, donde se administraron 70 Gy.
Tabla 2. Resultados respecto a los grados de dermatitis y prurito según las etapas de tratamiento radioterápico.
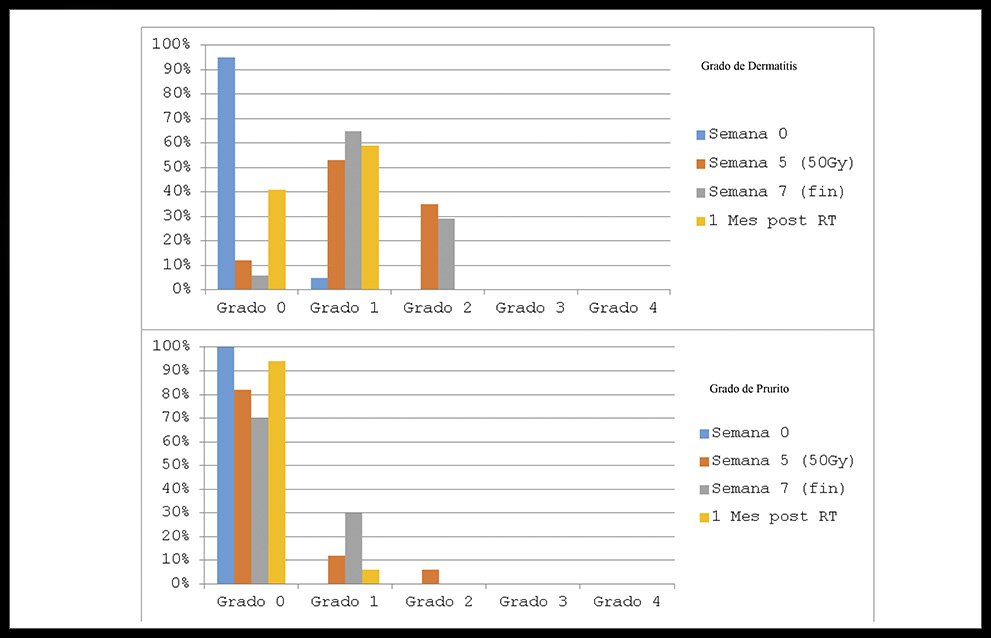
Figura 3. Grados de dermatitis y prurito en cada etapa del tratamiento radioterápico.
4. Valoración de los pacientes
Todos los pacientes que terminaron el estudio (N=17), contestaron un cuestionario administrado para la valorar la crema en relación a características organolépticas y de uso como: absorción, aroma, sensación de frescor, efectividad subjetiva, comodidad de administración y tolerabilidad (Tabla 3). La valoración se realizó bajo una puntuación de 0 a 10, siendo 10 la máxima puntuación y 0 la mínima.
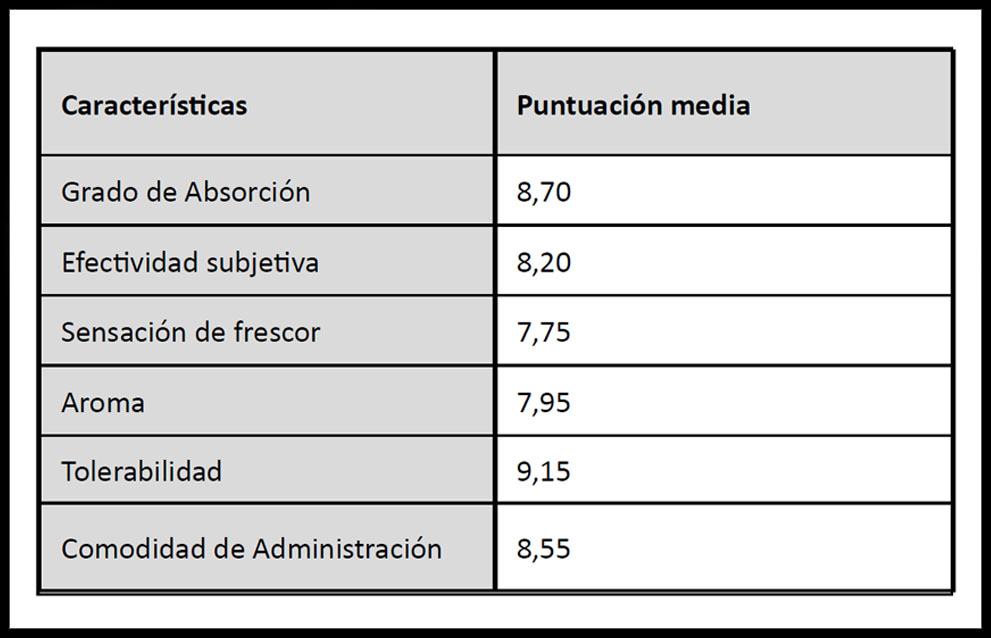
Tabla 3. Valoración Subjetiva de las características Radio Cream®.
Se observa como el ítem mejor valorado es la tolerabilidad con un 9,15 de puntuación media.
Respecto a la efectividad subjetiva, comodidad de administración y grado de absorción, obtienen puntuaciones muy similares y superiores a 8 (8.70 y 8.20), en sensación de frescor y aroma se ha obtenido la puntuación de 7.75 y 7.95 respectivamente y en cuanto a la comodidad a la hora de aplicar la crema, un 8.55.
5. Seguridad
Radio Cream® ha sido muy bien tolerada. No obstante, tres pacientes, de los 20 iniciales fueron excluidos. Un paciente presentó prurito durante la semana 3ª, en la zona de tratamiento, coincidiendo con la administración de la crema con dosis de 24 Gy., lo que obligó a suspender su administración al valorarse como probable reacción alérgica. Los síntomas desaparecieron al suspenderse la aplicación de la crema e iniciar tratamiento sistémico antihistamínico y corticoideo. Los 2 pacientes restantes que suspendieron el tratamiento, presentaron prurito grado 2 no controlado con la crema del estudio e iniciaron un tratamiento tópico con corticoides. No se apreció ningún efecto secundario a largo plazo, pudiendo el resto de los pacientes finalizar el tratamiento previsto.
DISCUSIÓN
La dermatitis por radiación sigue siendo la complicación aguda más común originada por el tratamiento radioterápico (2). El proceso del daño cutáneo inducido por la radiación está mediado por radicales libres que causan lesiones en el DNA, seguido por migración de células inflamatorias y lesión tisular (3). Aunque la fisiopatología y el mecanismo biológico subyacente aún no se comprenden por completo, se considera que los factores de crecimiento promueven la cicatrización de las heridas estimulando la proliferación celular (16). El EGF es uno de los factores clave del crecimiento tisular, estimulando la proliferación de los fibroblastos y queratinocitos durante el proceso de reparación (17;18).
En la práctica, el uso de EGF tópico ha demostrado su eficacia y a efectividad en el proceso de curación después de la radiodermatitis en diversos modelos preclínicos o clínicos (19-21).
En la actualidad existe alguna evidencia suficiente, para el uso estándar de cremas a base de EGF para el tratamiento de la dermatitis por RT (4;22;23). Algunos ensayos aleatorizados de fase III han informado un efecto preventivo superior de agentes tópicos, como corticosteroides (24), caléndula (25) y apósitos con base de nitrato de plata (26), para prevenir el desarrollo de la dermatitis. Sin embargo, el uso de esteroides tópicos es controvertido porque esto puede causar atrofia cutánea y favorecer la infección bacteriana. Las pomadas con base de caléndula no son fácilmente administrables por su viscosidad y alta densidad que dificulta su absorción y los apósitos con base de plata por la dificultas para aplicarlos por parte del paciente y la necesidad de retirada para la realización del tratamiento diario.
Una de las principales preocupaciones a la hora de utilizar EGF sería su posible efecto como potenciador tumoral. Existen informes que indican que el EGF administrado de forma exógena no estimula la proliferación de las células tumorales en ratones portadores de tumores (27), pero otros informes han demostrado resultados opuestos (28;29). La proporción de EGF en Radio Cream®, es muy inferior a la concentración de EGF de 15 μg utilizada en estudios previos (28); por lo tanto, suponemos que la aplicación local de Radio Cream® es segura. Además, no se encontró evidencia en la revisión de la literatura, que indicara que el EGF inició la tumorogénesis (30) y se infiere que la carcinogénesis no es una preocupación significativa en la aplicación tópica de EGF.
A pesar de las posibilidades que ofrece la aplicación de EGF, se han llevado a cabo escasos estudios sobre su utilidad en la prevención de la dermatitis por radiación. En 2014, Kang y colaboradores (26), presentaron un ensayo multicéntrico desarrollado en Corea usando una crema con base de EGF e incluyendo a 1,172 pacientes donde la incidencia de la dermatitis por radiación después de la RT fue del 46.6% (grado 1), 18.0% (Grado 2), 5.5% (Grado 3) y 0.9% (grado 4).
En el presente estudio piloto, la incidencia de la dermatitis por radiación después de la RT fue en el momento del primer corte (50 Gy.) del 12%, 53%, 35% de grado 0 al grado 2. No se observaron toxicidades grado 3 ni 4, lo que podría ser debido al bajo número de pacientes reclutados y a los criterios utilizados para valoración de las toxicidades en comparación con el estudio de Kang (26). Por otra parte, se observa una rápida recuperación de la irritación cutánea y sus síntomas, clasificándolas en grado 0:41%, grado 1:59% un mes finalizado el tratamiento, tiempo durante el cual, los pacientes continuaron con la administración de la crema.
Respecto al prurito, fue grado 0:70% y grado 1:30%, al finalizar el tratamiento, lo que nos permite valorar, que la crema Radio Cream®, ejerció una buena prevención, a pesar de la paciente que suspendió el tratamiento por reacción alérgica y las 2 pacientes que lo suspendieron por prurito no controlado con Radio Cream®.
De manera similar, la rápida recuperación de la dermatitis en los pacientes que finalizaron el estudio, respalda el efecto positivo del EGF. Además, el desarrollo de dermatitis por radiación fue independiente de la dosis total de radiación, y del fraccionamiento administrado, lo que podría valorarse como efecto preventivo del EGF ante la RT como concluía el estudio mencionado anteriormente de Kang (26).
La gran mayoría de pacientes expresaron una opinión muy positiva sobre parámetros físico-químicos-cosméticos de la crema, valores como la absorción, frescor y eficacia superaron de media una puntuación de 8 sobre 10, por otra parte, el aroma y sensación de frescor con la administración, fueron los menos valorados, pero superando el 7 de puntuación media.
El tratamiento fue bien tolerado y no se observaron efectos adversos graves ni mortalidad en la población estudiada, únicamente una paciente debió suspender el tratamiento por reacción alérgica, aunque la paciente no refería antecedentes de dicha patología.
Los pacientes que contestaron el cuestionario de valoración, consideraron que han tolerado el tratamiento. Esto ha permitido administrar sin interrupciones, la dosis planificada. La menor puntuación es 7,75 en sensación de frescor que les produce la crema. Este parámetro podría estar influenciado por la época del año en la que se desarrolló el estudio (otoño – invierno), cuando el clima es más frío. Además, la mayoría de los pacientes se administraban Radio Cream® a primera hora de la mañana y última del día, precisamente cuando la sensación térmica es menor.
CONCLUSIÓN
Aunque limitado por el número de pacientes y no ser un estudio aleatorizado utilizando un grupo control, se estima que la crema Radio Cream® de Inves Biofarm se ha mostrado como una opción válida para la prevención de la radiodermatitis. Esta crema con base de EGF puede impedir o retrasar la aparición de la toxicidad cutánea, así como reducir de una forma manifiesta la intensidad de la misma, contribuyendo así, al mantenimiento de la calidad de vida de los pacientes y permitir completar el tratamiento radioterápico a las dosis prescritas.
Es necesario validar mediante la inclusión de un mayor número de pacientes en el estudio y la realización de ensayos clínicos que certifiquen los resultados obtenidos en el presente estudio.
REFERENCE LIST
- Singh M, Alavi A, Wong R, Akita S. Radiodermatitis: A Review of Our Current Understanding. Am J Clin Dermatol 2016 Jun;17(3):277-92.
- Hickok JT, Morrow GR, Roscoe JA, Mustian K, Okunieff P. Occurrence, severity, and longitudinal course of twelve common symptoms in 1129 consecutive patients during radiotherapy for cancer. J Pain Symptom Manage 2005 Nov;30(5):433-42.
- Hymes SR, Strom EA, Fife C. Radiation dermatitis: clinical presentation, pathophysiology, and treatment 2006. J Am Acad Dermatol 2006 Jan;54(1):28-46.
- Chan RJ, Larsen E, Chan P. Re-examining the evidence in radiation dermatitis management literature: an overview and a critical appraisal of systematic reviews. Int J Radiat Oncol Biol Phys 2012 Nov 1;84(3):e357-e362.
- Lee J, Park W, Choi DH, Huh SJ, Kim IR, Kang D, et al. Patient-reported symptoms of radiation dermatitis during breast cancer radiotherapy: a pilot study. Qual Life Res 2017 Jul;26(7):1713-9.
- Wong RK, Bensadoun RJ, Boers-Doets CB, Bryce J, Chan A, Epstein JB, et al. Clinical practice guidelines for the prevention and treatment of acute and late radiation reactions from the MASCC Skin Toxicity Study Group. Support Care Cancer 2013 Oct;21(10):2933-48.
- McQuestion M. Evidence-based skin care management in radiation therapy. Semin Oncol Nurs 2006 Aug;22(3):163-73.
- Kumar S, Juresic E, Barton M, Shafiq J. Management of skin toxicity during radiation therapy: a review of the evidence. J Med Imaging Radiat Oncol 2010 Jun;54(3):264-79.
- Cornejo Uribe R. Epidermal Growth Factor and Mammary Epithelial Differentiation. Int.J.Morphol [29(3)], 821-824. 9-9-2011.
- Carpenter G, Cohen S. Epidermal growth factor. Annu Rev Biochem 1979;48:193-216.
- Inves-Biofarm. INFORME DE SEGURIDAD. sh-oligopeptide-1. 1-5.
- Vaughn AR, Clark AK, Sivamani RK, Shi VY. Natural Oils for Skin-Barrier Repair: Ancient Compounds Now Backed by Modern Science. Am J Clin Dermatol 2018 Feb;19(1):103-17.
- Rouvrais C, Bacqueville D, Bogdanowicz P, Haure MJ, Duprat L, Coutanceau C, et al. A new dermocosmetic containing retinaldehyde, delta-tocopherol glucoside and glycylglycine oleamide for managing naturally aged skin: results from in vitro to clinical studies. Clin Cosmet Investig Dermatol 2017;10:35-42.
- Cox JD, Stetz J, Pajak TF. Toxicity criteria of the Radiation Therapy Oncology Group (RTOG) and the European Organization for Research and Treatment of Cancer (EORTC). Int J Radiat Oncol Biol Phys 1995 Mar 30;31(5):1341-6.
- Porock D, Kristjanson L. Skin reactions during radiotherapy for breast cancer: the use and impact of topical agents and dressings. Eur J Cancer Care (Engl ) 1999 Sep;8(3):143-53.
- Denham JW, Hauer-Jensen M. The radiotherapeutic injury–a complex ‘wound’. Radiother Oncol 2002 May;63(2):129-45.
- Olascoaga A, Vilar-Compte D, Poitevin-Chacon A, Contreras-Ruiz J. Wound healing in radiated skin: pathophysiology and treatment options. Int Wound J 2008 Jun;5(2):246-57.
- Haubner F, Ohmann E, Pohl F, Strutz J, Gassner HG. Wound healing after radiation therapy: review of the literature. Radiat Oncol 2012 Sep 24;7:162.
- Lee SW, Jung KI, Kim YW, Jung HD, Kim HS, Hong JP. Effect of epidermal growth factor against radiotherapy-induced oral mucositis in rats. Int J Radiat Oncol Biol Phys 2007 Mar 15;67(4):1172-8.
- Wu HG, Song SY, Kim YS, Oh YT, Lee CG, Keum KC, et al. Therapeutic effect of recombinant human epidermal growth factor (RhEGF) on mucositis in patients undergoing radiotherapy, with or without chemotherapy, for head and neck cancer: a double-blind placebo-controlled prospective phase 2 multi-institutional clinical trial. Cancer 2009 Aug 15;115(16):3699-708.
- Ryu SH, Kim YH, Lee SW, Hong JP. The preventive effect of recombinant human growth factor (rhEGF) on the recurrence of radiodermatitis. J Radiat Res 2010;51(5):511-7.
- Zhang Y, Zhang S, Shao X. Topical agent therapy for prevention and treatment of radiodermatitis: a meta-analysis. Support Care Cancer 2013 Apr;21(4):1025-31.
- Schmuth M, Wimmer MA, Hofer S, Sztankay A, Weinlich G, Linder DM, et al. Topical corticosteroid therapy for acute radiation dermatitis: a prospective, randomized, double-blind study. Br J Dermatol 2002 Jun;146(6):983-91.
- Pommier P, Gomez F, Sunyach MP, D’Hombres A, Carrie C, Montbarbon X. Phase III randomized trial of Calendula officinalis compared with trolamine for the prevention of acute dermatitis during irradiation for breast cancer. J Clin Oncol 2004 Apr 15;22(8):1447-53.
- Niazi TM, Vuong T, Azoulay L, Marijnen C, Bujko K, Nasr E, et al. Silver clear nylon dressing is effective in preventing radiation-induced dermatitis in patients with lower gastrointestinal cancer: results from a phase III study. Int J Radiat Oncol Biol Phys 2012 Nov 1;84(3):e305-e310.
- Kang HC, Ahn SD, Choi DH, Kang MK, Chung WK, Wu HG. The safety and efficacy of EGF-based cream for the prevention of radiotherapy-induced skin injury: results from a multicenter observational study. Radiat Oncol J 2014 Sep;32(3):156-62.
- Choi J, Moon SY, Hong JP, Song JY, Oh KT, Lee SW. Epidermal growth factor induces cell death in the absence of overexpressed epidermal growth factor receptor and ErbB2 in various human cancer cell lines. Cancer Invest 2010 Jun;28(5):505-14.
- Geissler C, Hambek M, Eckardt A, Arnoldner C, Diensthuber M, Stover T, et al. The role of recombinant epidermal growth factor and serotonin in the stimulation of tumor growth in a SCCHN xenograft model. Oncol Rep 2012 Sep;28(3):785-90.
- Ginsburg E, Vonderhaar BK. Epidermal growth factor stimulates the growth of A431 tumors in athymic mice. Cancer Lett 1985 Sep 15;28(2):143-50.
- Berlanga-Acosta J, Gavilondo-Cowley J, Lopez-Saura P, Gonzalez-Lopez T, Castro-Santana MD, Lopez-Mola E, et al. Epidermal growth factor in clinical practice – a review of its biological actions, clinical indications and safety implications. Int Wound J 2009 Oct;6(5):331-46.
INFORMACIÓN DEL ARTÍCULO
Conflicto de interés: Los autores del presente trabajo declaran no tener conflicto de interés alguno.
Agradecimientos: Agradecemos a Melpopharma la ayuda con las traducciones y al Dr. J.P. García Corpas por el soporte técnico.
Autor para la correspondencia: María Fernández Rodríguez. Facultad de Farmacia, Universidad de Granada. Avda. de la Investigación, 11 · 18016 (Granada)