Caso Clínico
Conversión tardia por crecimiento continuado del saco aneurismático
Late open conversion due to countinous sac enlargement
Actual. Med. 2015; 100: (796). Supl. 14-36
RESUMEN
Desde hace dos décadas, el desarrollo de la tecnología endovascular ha revolucionado el manejo del aneurisma aórtico abdominal (AAA) demostrando una disminución de la morbi-mortalidad en los primeros 30 días. Las prótesis endovasculares requieren un estricto control radiológico y clínico a largo plazo para detectar las complicaciones que puedan generar una ruptura tardía del aneurisma. Aunque muchas de estas complicaciones pueden resolverse de forma endovascular, cada vez hay más casos en los que es necesario la conversión a cirugía abierta, aumentando así la mortalidad del procedimiento.
En este artículo se presenta el caso de una endoprótesis aórtica abdominal colocada en 2010, que, tras la aparición en dos ocasiones de endofugas con posterior aumento del saco aneurismático, cinco años después requiere conversión a cirugía abierta convencional como reparación.
Palabras clave: aneurisma, tratamiento endovascular, conversión a cirugía abierta
ABSTRACT
The development of endovascular techniques over the past two decades, has revolutionized the management of aortic aneurysms reducing postoperative morbidity and mortality significantly. Endovascular grafting requires strict radiological and clinical follow-ups in the long term in order to detect complications that may potentially cause aortic ruptures. Although many of complications may be solved through endovascular repair, conversión to open surgery is becoming more frequent, increasing mortality rates. This article reports a case os a complication after EVAR, in which the aneurysm sac was expanding due to endoleak, requiring new endografts in two occasions and conversión to open repair five years later the first endovascular repair.
Keywords: aneurysm, endovascular grafting, open conversión
Leer Artículo Completo
INTRODUCCIÓN
La reparación endovascular de aneurismas de aorta abdominal (Endovascular Aneurysm Repair, EVAR) ha ganado popularidad rápidamente como alternativa a la cirugía abierta convencional, probando ser seguro y efectivo en más de 90 % de casos¹, Debido al gran avance tecnológico, el EVAR se ha convertido en la primera opción terapéutica en pacientes con morfología aortoiliaca favorable². El EVAR presenta numerosas ventajas frente a la cirugía abierta como la disminución del tiempo quirúrgico y de hospitalización, rápida recuperación postquirúrgica y disminución de la morbimortalidad temprana tras intervención. La principal preocupación de esta técnica es la durabilidad de la endoprótesis a largo plazo y la aparición de complicaciones que requieran reintervenciones posteriores. Muchas de las complicaciones se manejan de forma endovascular pero, cada vez hay más reportes de pacientes que requieren conversión a cirugía por diversos motivos(2,3). La incidencia de conversión secundaria se encuentra entre 0,7-4%² y el riesgo aumenta con el tiempo. La mortalidad de estos procedimientos es mayor que en cirugía aórtica primaria convencional o prótesis endovascular, oscilando entorno al 20% (3,4).
CASO CLÍNICO
Se presenta un paciente varón de 80 años, como antecedentes de interés presenta fibrilación auricular anticoagulada, enfermedad coronaria con triple bypass aorto-coronario y disfunción ventricular ligera, exfumador desde hace 20 años, hábito enólico moderado y hepatopatía crónica por virus C.
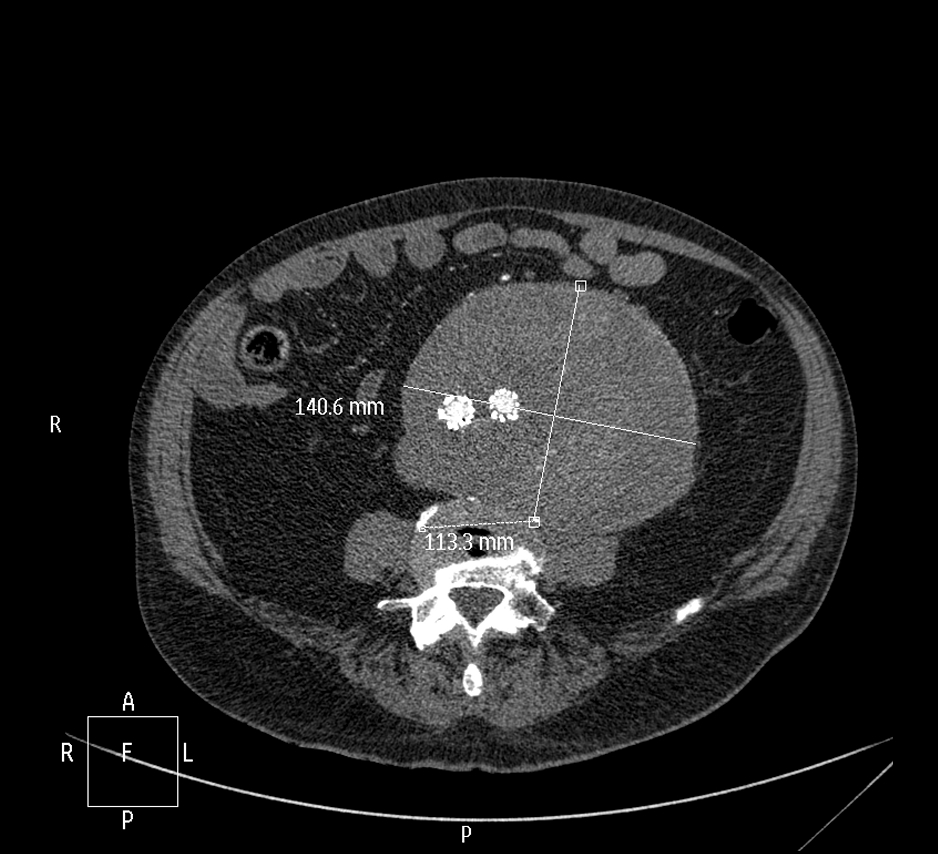
En 2003 tras la realización de un TAC de abdomen, se objetiva casualmente un AAA de 3,5cm (eje transverso) por lo que se sigue en consulta externa de cirugía vascular en otro hospital hasta que en 2005 se interviene de un AAA infrarrenal de 5,5cm mediante una endoprótesis bifurcada Talent®. En 2010, tras la realización de un angioTAC de control se halla un aumento del saco aneurismático de 10cm por posible endofuga tipo III por lo que se implantan extensiones iliacas Endurant® en cada rama de la prótesis bifurcada y se embolizan ramas de ambas arterias hipogástricas. De 2010 a 2013 el paciente es seguido en consulta externa de nuestro hospital sin evidencia de complicaciones y presentando un aumento del saco aneurismático a 11,5cm. En febrero de 2014 ingresa de forma urgente tras dolor brusco abdominal; se realiza un angioTAC evidenciándose un crecimiento del saco de 1cm en los últimos dos meses (12,5cm diámetro transverso) y hematoma periadventicial aórtico extendido a iliaca izquierda sin fuga activa, explicándose por posible fuga tipo IB sellada (Figura 1). Se reinterviene mediante una extensión Endurant II® a arteria Iliaca Externa derecha. En angioTAC de control al mes se observa disminución de la colección adventicial sin modificaciones del saco. En Septiembre, paciente asintomático y en TAC de control desaparece la colección periprotésica pero se objetiva un aumento del saco de 0,5cm sin fuga activa sospechándose una posible endotensión (endofuga tipo V).
Figura 1.
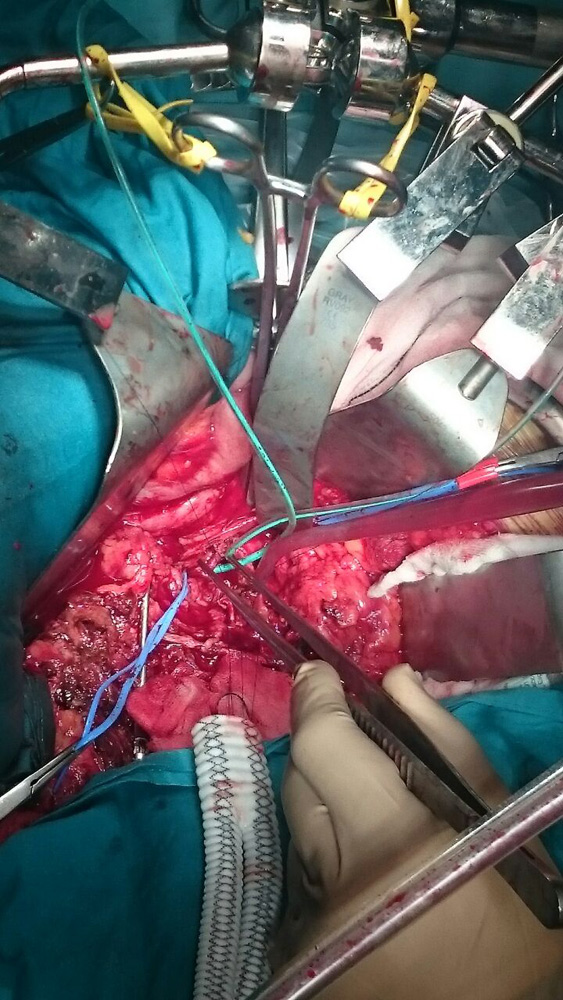
En mayo de 2015, el paciente continúa asintomático, en angioTAC presenta aumento del saco (14cm eje transverso) y extravasación de contraste en la vertiente posterolateral derecha del mismo a nivel de L5 por posible endofuga (Figura 2). Tras los nuevos hallazgos y el fallo de la reparación endovascular previa, se opta por conversión abierta tardía y explante de endoprotesis. En Julio de 2015 se procede de forma programada a realizar resección del AAA y explante de la endoprótesis con posterior colocación de un bypass aortobililiaco Dacron® 18×9 (Figura 3).
Figura 2.
Figura 3.
En postoperatorio inmediato presenta shock hemorrágico que necesita reintervención, evidenciándose gran trombo retroperitoneal y sangrado activo de arteria lumbar que se sutura. Posteriormente, Insuficiencia Renal tras anulación del riñón izquierdo por falta de flujo, hiperbilirrubinemia a expensas de la directa con ecografía normal, primera descompensación hidrópica con salida de líquido ascítico por laparotomía media intervenido por Cirugía General, edema agudo de pulmón y bacteriemia por Pseudomonas Aeruginosa como posible foco el catéter venoso central. Tras 5 días en la unidad de reanimación postquirúrgica y 23 días de cuidados en planta con manejo multidisciplinar estrecho, se procede al alta hospitalaria y seguimiento en consulta externa de nuestro servicio. Tres meses después, el paciente acude a urgencias por shock séptico tras peritonitis bacteriana, falleciendo a las 10 horas de ingreso.
DISCUSIÓN
El objetivo principal del tratamiento de AAA infrarrenal es prevenir su ruptura y el sustancial riesgo de muerte inminente asociado⁵. En las últimas décadas, el EVAR se ha establecido como alternativa segura y efectiva a la reparación abierta convencional, sobretodo en pacientes con edad avanzada o disfunción cardiaca, renal o pulmonar, disminuyendo así la morbimortalidad temprana asociada a la intervención (2).
La mayor limitación de esta técnica es la necesidad de seguimiento a largo plazo mediante técnicas de imagen debido a la alta tasa de complicaciones tardías que presenta, principalmente se trata de endofugas, migraciones de prótesis, ruptura de prótesis o trombosis intraprotésica. Las endofugas son las más frecuente (17% aproximadamente) y pueden ser de 5 tipos diferentes (2,5,6,7); en nuestro caso el paciente sufrió tres tipos diferentes de éstas durante 9 años de seguimiento tras la intervención. La mayoría de estas complicaciones, sobretodo aumento del saco aneurismático por porosidad de la prótesis o migración de ésta, se han descrito con prótesis de primera generación como Excluder® de Gore o Talent® de Medtronic (en nuestro paciente se colocó esta endoprótesis), siendo menos frecuentes en las prótesis de segunda generación actuales (1).
La mayoría de estas complicaciones se pueden reparar mediante la técnica endovascular. Sin embargo, en un pequeño porcentaje de casos (0-9% según diferentes series (1,4) la vía endovascular no está indicada o ha fallado previamente y requieren conversión a cirugía abierta. La necesidad de conversión de un procedimiento endovascular abdominal aórtico se clasifica en temprano, primeros 30 días tras la cirugía, o tardío, después de los 30 días³. La incidencia de conversión temprana es del 1,4% y se debe a complicaciones intraoperatorias principalmente, como la ruptura del aneurisma, mala posición de la endoprótesis, importante calcificación del cuello y fallo en el cateterismo de la rama contralateral. Esta incidencia tiende a disminuir cuando mejora la habilidad de los cirujanos vasculares y con la adecuada selección de los dispositivos y pacientes². La incidencia de conversión tardía varía entre 0 a 9% (1,4), las principales indicaciones: fugas, trombosis, migración, desconexión de ramas, infección del dispositivo o ruptura aneurismática de presentación aguda (1,3). En nuestro caso, tras diversas reparaciones endovasculares por la aparición de endofugas, se optó por conversión abierta tardía tras aumento persistente del saco hasta 14cm de diámetro transversal.
El procedimiento quirúrgico de explante de una endoprótesis es difícil y técnicamente muy exigente (3); el cirujano se enfrenta a un territorio hostil debido a la inflamación periaóritca producida por la endoprótesis, a la presencia de un aneurisma que no disminuyó de tamaño y a las dificultades en la extracción de dispositivos con fijaciones a la pared arterial. Por ello, el riesgo de sangrado por lesiones vasculares de la aorta y sus ramas, o la vena cava y las renales, es alto (8).
Para disminuir el riesgo de sangrado se utilizan diferentes técnicas como el control vascular suprarrenal por encima del tronco celiaco antes de la disección infrarrenal, como en este caso. Además de medidas de preservación de sangre, como la hemodilución normovolémica o la transfusión de reserva de hemoderivados, para minimizar las pérdidas hemáticas (1). En este caso, se utilizó un autotransfusor intraoperatorio. Sin embargo, a pesar de la correcta reposición sanguínea, ayuda postoperatoria con drogas vasoactivas y correcta hemostasia durante la técnica, requirió reintervención en pocas horas tras shock hemorrágico por sangrado activo a través de una rama lumbar que no se evidenció durante la reparación.
El éxito en el procedimiento de retirada de una endoprótesis aórtica depende del conocimiento de la prótesis a retirar, evaluar muy bien las imágenes diagnósticas y hacer abordajes quirúrgicos amplios. (1,2,3,4,8). En la mayoría de estudios de conversión prefieren procedimientos por vía transabdominal, tal y como fue en nuestro caso. Los estudios que comparan ambas vías informan de la disminución no significativa de íleo postquirúrgico en la vía retroperitoneal y mayor incidencia de hernias postquirúrgicas de la incisión abdominal en el abordaje transabdominal (1,4,8). Nuestro paciente tras ambas intervenciones, presentó evisceración de la pared abdominal en la región de la incisión media así como dehiscencia de ésta con salida de ascitis que requirió reparación por parte de cirugía general.
Actualmente se recomiendan procedimientos dejando piezas de endoprótesis funcionantes y sin fugas para disminuir el riesgo de sangrado y disección quirúrgica. En el presente caso se decidió explante completo de la endoprótesis, debido a los antecedentes de aparición de varias endofugas a lo largo del tiempo y al persistente aumento del tamaño del saco sin evidenciar fuga. En conclusión, la conversión abierta tardía tras EVAR puede ser exitosa y segura en algunos casos y se justifica el seguimiento imaginológico y clínico a largo plazo tras EVAR (9). Los factores clave que influyen en un resultado positivo son el adecuado estudio prequirúrgico individualizado, una adecuada indicación para la conversión, exitosa experiencia del cirujano en la técnica quirúrgica, el lugar de clampaje y la retirada parcial o completa del dispositivo. En nuestro centro, preferimos la retirada completa de prótesis si es posible aunque no siempre es necesario a no ser que la causa sea infección de ésta.
REFERENCIAS
- Jiménez CE, Correa JR, Burgos R. Conversión tardía de una endoprótesis aórtica a cirugía abierta: ¿se debe extraer toda la endoprótesis? Rev Colomb Cir. 2013; 28:48-53.
- Botsin S, Bausback Y, Piorkowski M et al. Late open conversion after endovascular aneurysm repair. Interact CardioVasc Thorac Surg. 2014; 19:622-626.
- Sachin VP, Keldahl ML, Morasch MD et al. Late abdominal aortic endograft explants: Indications and outcomes. Surgery. 2011; 150:788-95.
- Kelso RL, Lyden SP, Butler B et al. Late conversion of aortic stent grafts. J Vasc Surg 2009; 49: 589-95.
- Bryce Y, Rogoff P, Romanelli D et al. Endovascular Repair of Abdominal Aortic Aneurysms: Vascular Anatomy, Device Selection, Procedure, and Procedure-specific Complications. Radiographics. 2015. 35: 593-615.
- Heikkinen MA, Arlo FR, Zarins CK, Surg Clin. What is the significance of endoleaks and endotension. Surg Clin North Am. 2004. 84(5): 1337-52.
- Zhou W, Blay JR, Varu V et al. Outcome and clinical significance of delayed endoleaks after endovascular aneurysm repair. J Vasc Surg. 2014. 59(4): 915-20.
- Murphy EH, Pak J, Zarins CK. Open surgical repair after failed endovascular aneurysm repair: is endograft removal necessary? J Vasc Surg. 2009. 50: 714-21.
- Clayton J, Brinster, Ronald M. Late open conversion and explantation of abdominal aortic stent grafts. J Vasc Surg 2011. 54: 42-7.
INFORMACIÓN DEL ARTÍCULO
Autor para la correspondencia: Victoria García Blanco. e-mail: victoriagarciablanco@outlook.es