Original
Anti-péptidos citrulinados cíclicos y factor reumatoide en la Artritis Reumatoide
Anti-cyclic citrullinated peptide antibodies and rheumatoid factor in Rheumatoid Arthritis
Actual Med. 2021; 106(813): 157-164 DOI: 10.15568/am.2021.813.or02
Recibido: 14/04/2021
Revisado: 22/04/2021
Aceptado: 15/07/2021
Resumen
Introducción: Para el diagnóstico de Artritis Reumatoide (AR), se emplean la detección de dos autoanticuerpos; el factor reumatoide (FR) y los anticuerpos anti-péptidos citrulinados cíclicos (APCC). La presencia de estos anticuerpos determina que la AR se clasifique como seropositiva o seronegativa con importantes implicaciones tanto en el desarrollo clínico como en el pronóstico de la enfermedad.
Objetivo: Valorar el papel de los APCC y el FR en el diagnóstico de la AR, así como su influencia en la instauración del tratamiento farmacológico.
Metodología: Se estudiaron 213 pacientes con sospecha clínica inicial de AR con determinaciones de FR y APCC. Se estudiaron su diagnóstico definitivo y el tratamiento farmacológico instaurado.
Resultados: 63 de 213 pacientes tuvieron diagnóstico definitivo de AR. El 77,8 % se clasificaron como seropositivos. La sensibilidad y especificidad fueron superiores en los APCC frente a FR. Inicialmente el FR presentó un escaso valor diagnóstico ya que resultó negativo en más de dos tercios de los pacientes con diagnóstico de AR. El ajuste preciso de su valor de referencia permitió su utilización como una herramienta diagnóstica útil. La presencia de anticuerpos en pacientes con AR influye en el tratamiento de elección con una mayor utilización de metotrexato frente a otros inmunosupresotres en los pacientes seropositivos.
Conclusiones: Los APCC presentaron mejores parámetros de validez de prueba diagnóstica que el FR. La presencia de anticuerpos en la AR influye en el tratamiento de elección posiblemente por la mayor severidad de la patología.
Palabras clave: Artritis Reumatoide; Anticuerpos anti-péptidos citrulinados cíclicos; Factor reumatoide.
Abstract
Introduction: For the diagnosis of Rheumatoid Arthritis (RA), the detection of the autoantibodies, rheumatoid factor (FR) and cyclic citrullinated peptide antibodies (APCC) are used. The presence of these antibodies determines that the RA is classified as seropositive or seronegative, with important implications both in the clinical development and in the prognosis of the disease.
Objective: To assess the role of APCC and RF in the diagnosis of RA, as well as its influence on the establishment of pharmacological treatment.
Methodology: We studied 213 patients with initial clinical suspicion of RA and with determinations of FR and APCC. Their definitive diagnosis and the pharmacological treatment established were studied.
Results: 63 of 213 patients had a definitive diagnosis of RA. 77.8% were classified as seropositive. The sensitivity and specificity were higher in the APCC compared to FR. Initially the RF presented a low diagnostic value since it was negative in more than two thirds of the patients with a diagnosis of RA. The precise adjustment of its reference value allowed its use as a useful diagnostic tool. The presence of antibodies in patients with RA influences the treatment of choice with an increased use of Methotrexate against other immunosuppressants in seropositive patients.
Conclusions: The APCC presented better parameters of diagnostic test validity than the RF. The presence of antibodies in RA influences the treatment of choice possibly due to the greater severity of the pathology.
Keywords: Anti- cyclic citrullinated peptide antibodies; Rheumatoid factor; Rheumatoid Arthritis.
Leer Artículo Completo
INTRODUCCIÓN
La Artritis Reumatoide (AR) es una enfermedad sistémica crónica, de naturaleza autoinmune, que se caracteriza por la inflamación y destrucción irreversible del cartílago articular y hueso subyacente. La enfermedad sigue un curso progresivo, que si no es tratada adecuadamente puede originar una importante discapacidad (1). Su característica principal es la presencia de inflamación sinovial persistente junto con daño articular (2).
La AR afecta principalmente a articulaciones de pequeño y mediano tamaño. Las articulaciones metacarpofalángicas y las interfalángicas proximales son las más comúnmente afectadas (3). En fases muy avanzadas de la enfermedad es cuando se pueden observar deformidades como consecuencia del daño y la destrucción articular. Las manifestaciones extraarticulares se suelen presentar en pacientes con AR de larga evolución y formas más severas.
Actualmente, los criterios de la EULAR (Liga Europea Contra Enfermedades Reumatológicas) /ACR (Colegio Americano de Reumatología) propuestos en el año 2010 son los utilizados para establecer el diagnóstico de la AR (3). Los criterios actuales difieren de los propuestos con anterioridad en plantear un diagnóstico más precoz de la enfermedad reduciendo así la destrucción articular y el daño generado, mediante la posibilidad de un inicio temprano del tratamiento. En la actualidad se dispone de un arsenal de tratamientos que permiten un adecuado control de la enfermedad (4,5).
La AR es una enfermedad de etiología autoinmune, en la que los dos anticuerpos más relevantes para el diagnóstico y manejo de la patología son el factor reumatoide (FR) y los anticuerpos anti-péptidos citrulinados cíclicos (APCC). En la guía diagnóstica de la EULAR/ACR 2010 la presencia de estos autoanticuerpos se estableció como criterio diagnóstico de la AR. El FR fue el primer anticuerpo descrito para la AR siendo un autoanticuerpo que se dirige contra la fracción constante de la IgG (6). La presencia de FR a pesar de su baja especificidad se incluyó ya en los criterios diagnósticos del año 1987 (7). Los APCC se dirigen contra proteínas citrulinadas, en las que se ha producido conversión del aminoácido arginina en citrulina mediante un proceso enzimático de citrulinación. Esta modificación postranslacional puede ser reconocida como extraña por el sistema inmunológico. Los APCC presentan frente al FR una elevada especificidad en la AR (8,9). Estos anticuerpos resultan muy útiles en estadios iniciales de la enfermedad en los cuales todavía no se cumplen criterios de AR, pero los APCC están presentes. A este síndrome se le denomina Artritis Indiferenciada. Dentro de estos pacientes, la gran mayoría (90%) desarrollará AR en los siguientes 3 años por lo que son muy buenos predictores de enfermedad (4). Los anticuerpos han demostrado preceder a la enfermedad y pueden ser detectados incluso 10 años antes de las manifestaciones clínicas (8). Junto con la detección precoz, estos anticuerpos también se han relacionado con el curso de la enfermedad y se ha demostrado que su concentración determina el grado de destrucción ósea (10).
Dentro de la AR se ha establecido una subdivisión en función de la presencia (AR seropositiva) o ausencia (AR seronegativa) de los autoanticuerpos (FR y/o APCC), ya que se consideran diferentes en cuanto a la progresión de la enfermedad, destrucción articular e incluso al tratamiento (11). Los sujetos seropositivos y, sobre todo, los que presentan APCC, tienen una progresión de erosiones y destrucción ósea más marcada que los seronegativos (10). Se sabe que los pacientes seropositivos presentan una mejor respuesta al metotrexato (MTX), mientras que los seronegativos no presentan tan buena respuesta al mismo tratamiento (12). El objetivo principal del presente trabajo es valorar el papel de los anticuerpos APCC y FR en el diagnóstico de la AR y su relación con los tratamientos farmacológicos.
MATERIAL Y MÉTODOS
Pacientes
Se trata de un estudio observacional, descriptivo y transversal. Se recogieron los datos de forma retrospectiva en el periodo comprendido entre febrero – abril de 2020. Se incluyen en el estudio a todos los pacientes con sospecha clínica de AR a los que se les solicitaron los anticuerpos característicos de la AR. Se excluyeron los pacientes a los que por cualquier causa no se pudieron recoger todas las variables diseñadas en el estudio. Finalmente se estudiaron 213 pacientes a los que se les solicitó un perfil de anticuerpos por sospecha clínica inicial de AR con resultados obtenidos tanto para FR como APCC en el laboratorio del Hospital General Universitario de Ciudad Real. Las variables se recogieron a partir de las historias clínicas y de los hallazgos bioquímicos/inmunológicos de los sujetos a estudio. Se recogieron las siguientes variables: sexo, edad del paciente, resultados de FR y de APCC, diagnóstico final, y en los pacientes con un diagnóstico de AR el tipo de la enfermedad (AR seropositiva o seronegativa), así como el tratamiento de base instaurado clasificados de la siguiente forma: Metotrexate (MTX), biológicos anti TNFα (adalimumab, certolizumab, golimumab, etanercept), y el resto de tratamientos modificadores de la enfermedad recogidos en el grupo otros (hidroxicloroquina, leflunomida…), además de todas sus combinaciones.
Todos los pacientes incluidos en el estudio dieron su consentimiento a participar después de haber sido informados de forma concienzuda acerca del estudio.
Determinación del FR
El método empleado mide la concentración de FR en suero mediante inmunoturbidimetría potenciada con látex (ADVIA XPT 2400 Siemens Healthcare, GER). Las partículas de látex recubiertas con el anticuerpo se aglutinan rápidamente en presencia del FR dando lugar a la formación de agregados por aglutinación. La aglutinación da lugar a un aumento de la turbidez que puede medirse mediante la dispersión de luz generada a 571 nm. La concentración de FR en el suero se determina a partir de una curva de calibración obtenida con un juego de calibradores. Se consideró positividad para el FR si la concentración en plasma de los pacientes era >60 UI/mL. Este valor de referencia es el fijado y empleado por el laboratorio de acuerdo con las recomendaciones de la casa suministradora del reactivo.
Valoración de los APCC
La presencia de APCC se determinó mediante enzimoinmunoensayo cuantitativo sobre pocillos recubiertos con péptidos que contienen residuos arginina modificados mediante citrulinación (Euroimmun, Lübeck GER). Como conjugado el equipo utiliza un anticuerpo policlonal de conejo anti-IgG humana conjugado con peroxidasa. Se utilizaron cinco calibradores con un rango de 1 a 500 U/mL. Como valor de referencia se utilizó el recomendado por el suministrador de los equipos considerando la presencia de APCC cuando el valor obtenido es > 5U/mL.
Análisis Estadístico
En cuanto a la valoración de parámetros de eficacia diagnóstica, se valoró el papel del FR y los APCC en el diagnóstico de la AR, teniendo en cuenta como patrón de referencia los resultados descritos en la bibliografía. Se identificaron los falsos negativos (FN), los falsos positivos (FP), los verdaderos negativos (VN) y los verdaderos positivos (VP), y se calcularon como parámetros de eficacia diagnóstica: sensibilidad (S): S= VP/(VP+FN); especificidad (E): E=VN/(VN+FP); valor predictivo positivo (VPP): VPP=VP/(VP+FP); valor predictivo negativo (VPN): VPN=VN/(FN+VN).
Las diferentes asociaciones entre parámetros cualitativos se estudiaron mediante la prueba de χ2 de Pearson, empleando el Test exacto de Fisher en los casos en los que se consideró necesario (observados y/o esperados < 5). Se consideraron resultados significativos los que obtuvieron un p-valor inferior a 0,05. Para la comparación de parámetros cuantitativos se empleó la prueba de la T de Student para muestras independientes. Se ha utilizado IBM SPSS Statistics versión 25 para el procesamiento estadístico de los datos.
RESULTADOS
Pacientes
Durante el periodo de estudio, por una sospecha diagnóstica de AR, se realizaron 213 solicitudes de anticuerpos APCC y FR. Ninguno de ellos tenía estudios previos. A 203 pacientes se le solicitaron determinación de ambos anticuerpos mientras que a los 10 restantes únicamente se les solicitaron los APCC. Del total de la muestra estudiada y de acuerdo con las historias clínicas, 63 pacientes (29,58%) se correspondieron a sujetos con un diagnóstico definitivo de AR de acuerdo con los criterios de la ACR (3), mientras que el resto 150 pacientes (70,42%) no cumplieron con los criterios diagnósticos de la enfermedad.
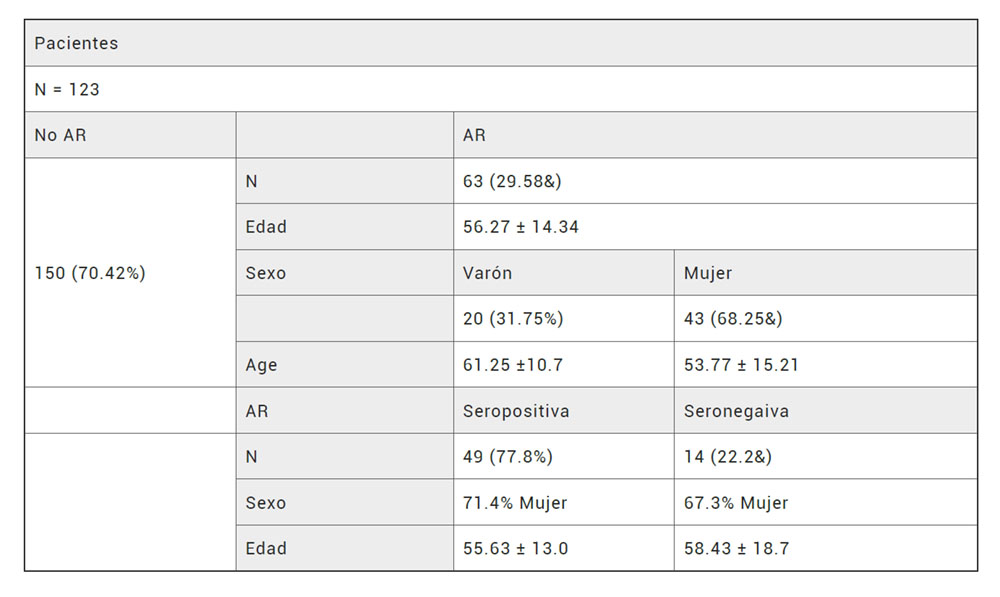
Los datos demográficos de los pacientes se muestran en la Tabla 1, y de ellos podemos destacar una mayor frecuencia del sexo femenino en los pacientes con diagnóstico de AR superando los dos tercios del total, y además con un inicio más precoz de la enfermedad, aproximadamente siete años antes que los varones.
Tabla 1. Datos demográficos de los pacientes incluidos en el estudio. Se desglosan los datos en función del diagnóstico de AR y si la enfermedad se clasifica como seropositiva o seronegativa en función de la presencia de anticuerpos (APCC y/o FR). El sexo se presenta en porcentajes y la edad en años ± desviación estándar.
Estudios de anticuerpos
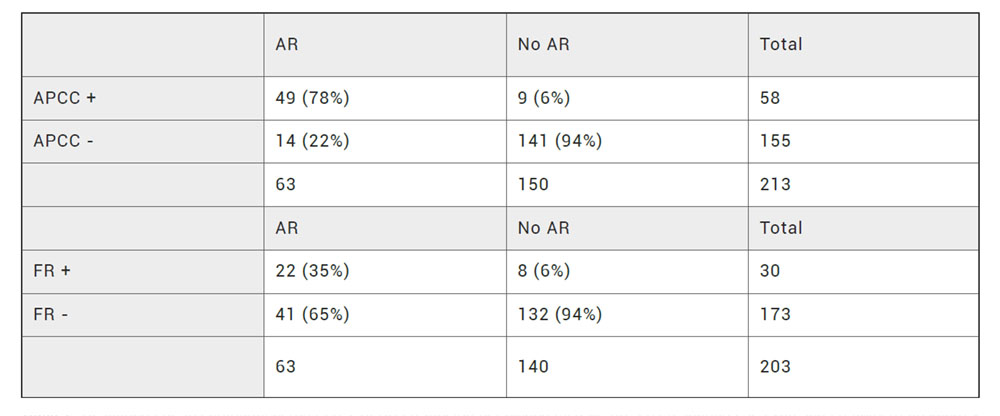
Los resultados obtenidos en los estudios de ambos anticuerpos en función del diagnóstico de AR se presentan en la Tabla 2.
Tabla 2. Resultados de los autoanticuerpos FR y APCC en función del diagnóstico de AR. Los resultados se expresan en número absoluto y porcentajes.
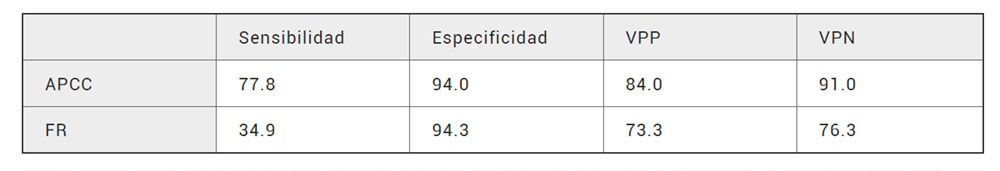
A partir de los datos descritos se obtuvieron los resultados de los parámetros de validez diagnóstica que se muestran en la Tabla 3.
Tabla 3. Parámetros de eficacia diagnóstica obtenidos a partir de los resultados de los anticuerpos FR y APCC y los diagnósticos de AR. Los resultados se expresan en porcentajes.
Los resultados obtenidos para los APCC concuerdan con lo descrito en otras series (10, 11), sin embargo, los resultados obtenidos para el FR muestran una muy baja sensibilidad por debajo del 35 %. que va asociada a una muy elevada especificidad. De los presentes datos se deduce que la prueba de FR, por si sola, descarta a un elevado número de potenciales pacientes con AR (falsos negativos).
La AR seropositiva se establece como la que presenta resultado positivo para alguno, o ambos, de estos dos autoanticuerpos. De los 63 pacientes con el diagnóstico de AR, se determinó que 49 de ellos (77,8%) corresponden a AR seropositivas, mientras que 14 (22,2%) pertenecen a AR seronegativas. En cuanto a la distribución por sexo, este resultó ser mucho más frecuente en mujeres en ambos serotipos de AR, pero sin diferencias significativas (p = 1), como se muestra en la Tabla 1.
Se observó una cierta predisposición con sujetos más jóvenes en la seropositiva, pero también sin significación estadística (p= 0,61).
Valores de referencia de FR
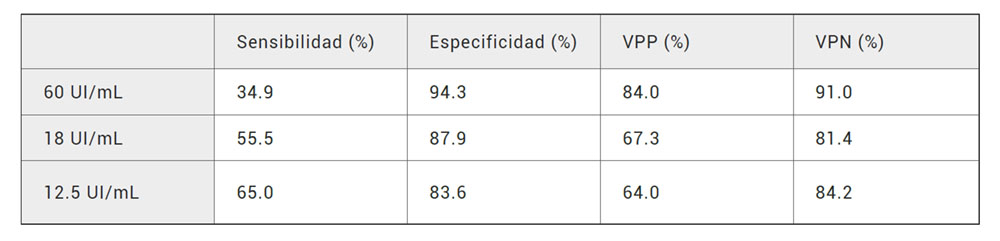
Debido a los resultados de sensibilidad tan bajos obtenidos para el FR se dedujo que el valor de referencia recomendado era excesivamente alto, por lo que se procedió determinar el valor adecuado para nuestra población. Para ello se realizó la determinación en 50 individuos sanos en los que previamente se descartó cualquier tipo de clínica y antecedentes familiares relacionados con conectivopatías. La media de FR obtenida fue 9,4 UI/mL ± 1,6. A partir de este dato se obtuvieron dos valores de referencia, utilizando el percentil 97,5 (18 UI/mL) y considerando la media ± 2 desviaciones estándar (12,5 UI/mL). Con estos nuevos valores de referencia se obtuvieron resultados para el FR con sensibilidades adecuadas para el diagnóstico de AR (Tabla 4) y similares a las descritas por otros autores. Las modificaciones del valor de referencia no afectaron a la determinación de seropositividad en la AR ya que todos los pacientes con FR positivo con los nuevos valores de referencia ya presentaban APCC positivos.
Tabla 4. Análisis de los parámetros de eficacia diagnóstica en función de los valores de referencia. El primero 60 U/mL es recomendado por el suministrador de los reactivos, el segundo 18 U/mL se obtiene a partir del percentil 97,5 a partir de la media obtenida en una población de 50 individuos sanos, y el tercero 12,5 U/mL se corresponde con la media ± dos desviaciones estándar. Los resultados se expresan en porcentajes.
Anticuerpos en entidades diferentes de la AR
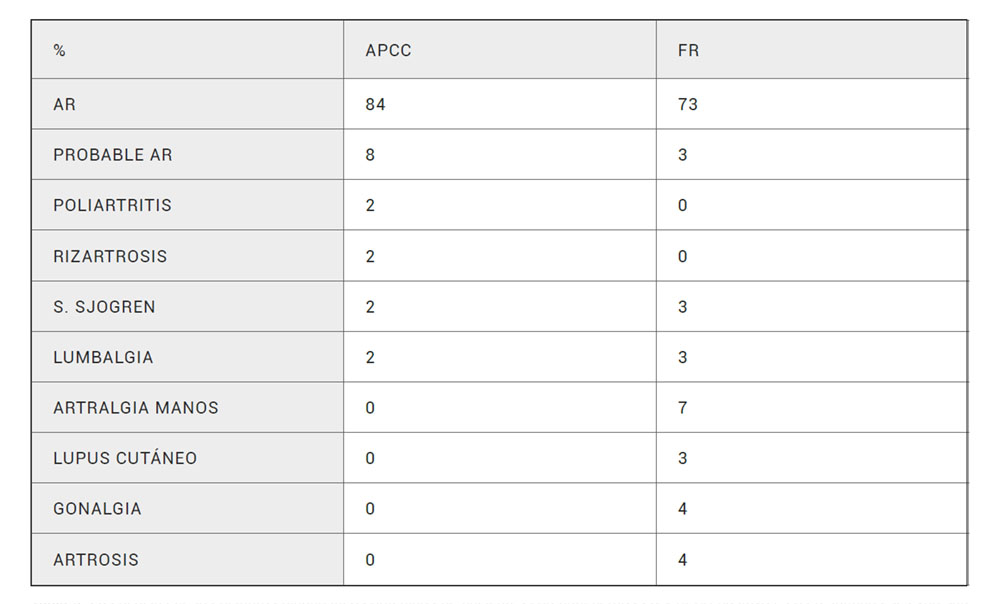
Los pacientes con APCC, en gran mayoría se corresponden con el diagnóstico de AR (84%). Sin embargo, existe un porcentaje que no corresponden con esta entidad. Muchos de estos diagnósticos no están del todo establecidos ya que su presencia se ha clasificado en “probable AR”, o poliartrosis, (Tabla 5). Las probables AR engloban entidades que, no cumpliendo criterios de AR, se asemejan mucho ya sea por sus manifestaciones clínicas o por su debut y que gran parte de ellas acaban desarrollando dicha enfermedad en un futuro.
Tabla 5. Frecuencias de los distintos diagnósticos obtenidos de pacientes con anticuerpos FR y APCC positivos. Los resultados se expresan en porcentajes.
En los pacientes con detección de FR el porcentaje de AR es menor que en los APCC (73%), sin embargo, la diversidad de patologías para este anticuerpo resulta mayor. Dentro de estas podemos encontrar enfermedades claramente definidas, como son el síndrome de Sjögren, lupus cutáneo o artrosis, pero también otras patologías con el diagnóstico poco conciso como ocurre con los APCC. Dentro de estos podemos destacar artralgias de manos, y otro grupo de entidades catalogadas como “probable AR” (Tabla 5).
Tratamientos en función de la presencia de anticuerpos
En relación con el tratamiento empleado para la AR, 25 pacientes (39,68%) están tratados con MTX en monoterapia, 11 con biológicos en monoterapia (17,46%), 11 con combinación de MTX y biológicos (17,46%) y 16 (25,4%) con otros fármacos como leflunomida, hidroxicloroquina y/o combinación con los anteriores. Se han excluido los corticoides junto con los AINES ya que se emplean para el control de los episodios agudos de la enfermedad en combinación con alguno de los fármacos anteriores.
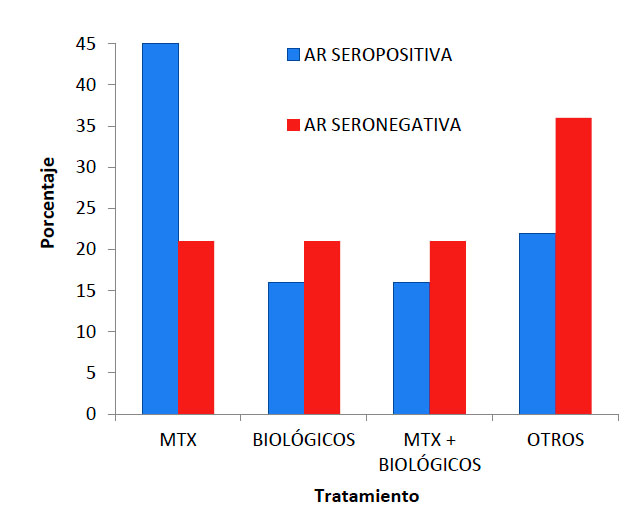
Si hacemos distinción entre sujetos AR seropositivos y seronegativos, casi la mitad (45%) de los seropositivos emplean el MTX en monoterapia frente a un 21% de los sujetos con AR seronegativa. En cambio, en estos últimos se emplean más el grupo “otros fármacos” en decremento del MTX como se muestra en la figura.1. No se observaron diferencias estadísticamente significativas, aunque si una tendencia a una mayor utilización de MTX frente a otros fármacos en el caso de AR seropositiva (p = 0,1).
Figura 1. Porcentaje de los tratamientos implantados a los pacientes de AR en función de la clasificación de la enfermedad en seropositiva o seronegativa de acuerdo con la presencia de los anticuerpos APCC y/o FR. Metotrexato (MTX), Biológicos (anti-TNFα), otros (leflunomida, hidroxicloroquina y combinación de los anteriores).
El presente trabajo ha sido aprobado por el comité de ética e investigación con medicamentos CEIm de la Gerencia de Atención Integrada de Ciudad Real.
DISCUSIÓN
La AR es una de las enfermedades autoinmunes más frecuente en la población general. La prevalencia en España es del 0,5% lo que supondría en torno a 235.000 casos en total en nuestro país (13). La detección precoz de la enfermedad resulta primordial ya que con una actuación en fases precoces de la enfermedad se puede evitar el curso progresivo de la enfermedad y sobre todo se pueden prevenir las secuelas invalidantes que genera la AR como consecuencia de las erosiones irreversibles (1). La detección de anticuerpos asociados a la AR puede ser una herramienta útil para un diagnóstico precoz y la iniciación de un tratamiento adecuado.
Los resultados presentados en el presente estudio para APCC concuerdan con lo descrito en otras series (8,9,14), pero en cambio los obtenidos par el FR mostraron una sensibilidad muy baja para utilizarse como una herramienta de diagnóstico precoz. Al establecer un elevado valor de referencia, según recomendación de la casa suministradora, la especificidad resultó mucho más elevada que lo descrito previamente (15), mientras que su sensibilidad resultó mucho más baja, dejando de forma hipotética a dos tercios de los potenciales pacientes con AR con resultados negativos para FR. Ante estos resultados se optó por ajustar el valor de referencia de la técnica a partir de nuestra población. Utilizando un valor de referencia adecuado, se consiguió una sensibilidad semejante a la de los APCC, aunque con una menor especificidad tal como se recogen en otros estudios, y de esta forma el FR pasa a ser una herramienta útil para un prediagnóstico de AR. El uso de valores de referencia adecuados y testados en nuestra población resulta indispensable para una adecuada interpretación de los resultados.
La menor especificidad del FR frente a APCC se traduce en que se obtuvo un menor porcentaje de pacientes sin diagnóstico de AR, pero con anticuerpo positivo (falso positivo) para los APCC (16 %) en comparación con FR (27%). Respecto a los APCC dentro de los diagnósticos que no correspondían a AR cumpliendo los criterios de la ACR 2010, se encuentran otros inespecíficos como son probable AR o poliartrosis que suponen un 10 % de los pacientes. La presencia de estos anticuerpos sugiere probablemente la denominada Artritis Indiferenciada”, por lo que es esperable que la mayoría de estos pacientes desarrollarán AR dentro de los próximos 3 años (4). Además, se observa cómo los APCC están presentes en un menor número de entidades diferentes a la AR. Esto no ocurre con el FR ya que su presencia en no diagnosticados de AR es mucho más variada, suponiendo un porcentaje mucho más bajo (3%) de Artritis Indiferenciada. Por el contrario, podemos encontrar FR en otras patologías claramente definidas, como síndrome de Sjögren, artrosis, gonalgia mecánica, y lupus cutáneo. Los APCC resultas más específicos para el diagnóstico de la AR que el FR.
Finalmente, si tenemos en cuenta el tratamiento empleado para la AR, hemos de destacar que el fármaco fundamental es el MTX. Sin embargo, su uso difiere en relación con el serotipo de la AR. En casi la mitad de los individuos seropositivos se consigue controlar la enfermedad con MTX en monoterapia. Este porcentaje es mayor si tenemos en cuenta que la mayoría de estos pacientes en caso de que el MTX no sea suficiente, se le añadirá otro fármaco a este para controlar la enfermedad. En el caso de la AR seronegativa, el porcentaje de uso del MTX disminuye hasta un 21%. Esto puede deberse a que en estos individuos se consiga controlar la enfermedad con el uso de otros inmunomoduladores, ya que sigue un curso totalmente diferente y generalmente no tiene un carácter tan agresivo como la AR seropositiva (12). Por tanto, se puede establecer que en la AR seropositiva se consigue una mejor respuesta con el MTX, ya sea en monoterapia o en combinación con otros fármacos. Por el contrario, en las AR seronegativas el tratamiento resulta más diverso, puesto que no hay una clara predilección por ninguno de los fármacos, debiéndose emplear el que consiga controlar la enfermedad atendiendo a las características clínicas del paciente. La presencia de autoanticuerpos en la AR se asocia con una mayor utilización de MTX como tratamiento de elección.
REFERENCIAS BIBLIOGRÁFICAS
- ↑ Scott DL, Wolfe F, Huizinga TW. Rheumatoid arthritis. Lancet. 2010; 376(9746): 1094–108. DOI: 10.1016/S0140-6736(10)60826-4
- ↑ Van Oosterhout M, Bajema I, Levarht EWN, Toes REM, Huizinga TWJ, van Laar JM. Differences in synovial tissue infiltrates between anti–cyclic citrullinated peptide–positive rheumatoid arthritis and anti–cyclic citrullinated peptide–negative rheumatoid arthritis. Arthritis Rheum. 2008; 58(1): 53–60. DOI: 10.1002/art.23148
- ↑ Aletaha D, Neogi T, Silman AJ, Funovits J, Felson DT, Bingham CO, et al. 2010 Rheumatoid arthritis classification criteria: An American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum. 2010; 62(9): 2569–81. DOI: 10.1002/art.27584
- ↑ Van der Helm-vanMil AHM, le Cessie S, van Dongen H, Breedveld FC, Toes REM, Huizinga TWJ. A prediction rule for disease outcome in patients with Recent-onset undifferentiated arthritis: How to guide individual treatment decisions. Arthritis Rheum. 2007; 56(2): 433–40. DOI: 10.1002/art.22380
- ↑ Wunderlich C, Oliviera I, Figueiredo CP, Rech J, Schett G. Effects of DMARDs on citrullinated peptide autoantibody levels in RA patients-A longitudinal analysis. Semin Arthritis Rheum. 2017; 46(6): 709–14. DOI: 10.1016/j.semarthrit.2016.09.011
- ↑ Anquetil F, Clavel C, Offer G, Serre G, Sebbag M. IgM and IgA rheumatoid factors purified from rheumatoid arthritis sera boost the Fc receptor- and complement-dependent effector functions of the disease-specific anti-citrullinated protein autoantibodies. J Immunol. 2015; 194(8): 3664–74. DOI: 10.4049/jimmunol.1402334
- ↑ Arnett FC, Edworthy SM, Bloch DA, McShane DJ, Fries JF, Cooper NS, et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum. 1988; 31(3): 315–24. DOI: 10.1002/art.1780310302
- ↑ Nielen MMJ, van Schaardenburg D, Reesink HW, van de Stadt RJ, van der Horst-Bruinsma IE, de Koning MHMT, et al. Specific autoantibodies precede the symptoms of rheumatoid arthritis: A study of serial measurements in blood donors. Arthritis Rheum. 2004; 50(2): 380–6. DOI: 10.1002/art.20018
- ↑ Zendman AJW, van Venrooij WJ, Pruijn GJM. Use and significance of anti-CCP autoantibodies in rheumatoid arthritis. Rheumatology. 2006; 45(1): 20–5. DOI: 10.1093/rheumatology/kei111
- ↑ van der Helm-van Mil AH, Verpoort KN, Breedveld FC, Toes RE, Huizinga TW. Antibodies to citrullinated proteins and differences in clinical progression of rheumatoid arthritis. Arthritis Res Ther. 2005; 7(5): R949. DOI: 10.1186/ar1767
- ↑ Derksen VFAM, Ajeganova S, Trouw LA, van der Helm-van Mil AHM, Hafström I, Huizinga TWJ, et al. Rheumatoid arthritis phenotype at presentation differs depending on the number of autoantibodies present. Ann Rheum Dis. 2017; 76(4): 716–20. DOI: 10.1136/annrheumdis-2016-209794
- ↑ van Dongen H, van Aken J, Lard LR, Visser K, Ronday HK, Hulsmans HMJ, et al. Efficacy of methotrexate treatment in patients with probable rheumatoid arthritis: A double-blind, randomized, placebo-controlled trial. Arthritis Rheum. 2007; 56(5): 1424–32. DOI: 10.1002/art.22525
- ↑ Carbonell J, Cobo T, Balsa A, Descalzo MA CLSSG. The incidence of rheumatoid arthritis in Spain: results from a nationwide primary care registry. Rheumatol (Oxford). 2008; 47(7): 1088–92. DOI: 10.1093/rheumatology/ken205
- ↑ Enriconi dos Anjos LM, Pereira IA, d ‘Orsi E, Seaman AP, Burlingame RW, Morato EF. A comparative study of IgG second- and third-generation anti-cyclic citrullinated peptide (CCP) ELISAs and their combination with IgA third generation CCP ELISA for the diagnosis of rheumatoid arthritis. Clin Rheumatol. 2009; 28(2): 153–8. DOI: 10.1007/s10067-008-0999-5
- ↑ Nielsen SF, Bojesen SE, Schnohr P NB. Elevated rheumatoid factor and long-term risk of rheumatoid arthritis: a prospective cohort study. BMJ. 2012; 345: e5244. DOI: 10.1136/bmj.e5244
INFORMACIÓN DEL ARTÍCULO
Conflicto de intereses: Los autores/as de este artículo declaran no tener ningún tipo de conflicto de intereses respecto a lo expuesto en el presente trabajo.
Autor para la correspondencia: José Miguel Urra Ardanaz Laboratorio de Inmunología. Hospital General Universitario de Ciudad Real · 13005, Ciudad Real, España. E-mail: josemiguel.urra@uclm.es