
140
Kevin Doello
Nanopartículasmagnéticas y cáncer
que pueden ser usadas, entre otras muchas aplicaciones, en el
campo de la oncología para mejorar el diagnóstico y tratamiento
de los tumores. Las nanopartículas (NPs), las más desarrolladas y
analizadas, pueden ser hidrófilas o lipofílicas. Las primeras están
constituidas por polímeros (NPs poliméricas) de ácido láctico-co-
glicólico (PLGA), epsilon- poli-caprolactona (PLC), chitosán o poli-
butil-cianocrilato (PBCA), entre otros; las segundas (NPs sólidas li-
pídicas) están compuestas por lípidos sólidos como por ejemplo el
tripalmitato. Aunque con características y propiedades diferentes,
su diseño atiende especialmente a la capacidad para transportar
de forma selectiva fármacos citotóxicos hacia las células tumorales
lo que redunda en una más efectiva destrucción de dichas células y
en una menor toxicidad de las drogas en los tejidos sanos, aumen-
tando por tanto su rango de seguridad (3). Un hecho fundamental
que explica esta última ventaja cuando se usan NPs, es el efecto de
retención y permeabilidad aumentadas o conocido también por su
siglas en inglés como efecto EPR (
enhanced permeability and re-
tention
) por el que la presencia de una abundante vascularización
inmadura en el tejido tumoral con grandes fenestraciones, hace
que en estos tejidos se acumulen mayor cantidad de NPs que en
los tejidos sanos y por tanto mayor cantidad de agentes citotóxicos.
Por tanto, los fármacos citotóxicos transportados por NPs poseen
mayor facilidad para alcanzar los tejidos tumorales que los mismos
fármacos administrados de forma libre lo que posiblemente explica
el mayor éxito de esta nueva estrategia terapéutica (4) (Figura 1).
Un aspecto esencial del uso de NPs en el tratamiento del
cáncer es la posibilidad de poder funcionalizarlas. Existen diversos
métodos para conseguir esta funcionalización, destacando aquel
por el que se une a la superficie de la NP determinadas moléculas
o ligandos, cuyos receptores diana se encuentran sobreexpresados
en células tumorales, permitiendo así la unión específica a esos re-
ceptores presentes en estos tipos celulares y por tanto mejorando
así el targeting entre ambos (Figura 1). Dentro del campo de la fun-
cionalización se encuentra la posibilidad de incluir en el centro de
la nanoplataforma, es decir, el nanotransportador de fármacos y
otras moléculas, núcleos magnéticos lo que implica repercusiones
específicas en cuanto al posible uso de las mismas (4). Esta modifi-
cación permite que puedan ser usadas como método de diagnós-
tico o también como sistema terapéutico en diversas patologías
entre las que se encuentra el cáncer. Su propiedad fundamental es
que, además de tener tendencia a localizarse en el tejido tumoral
(“
targeting
pasivo”), los núcleos magnéticos permiten direccionar-
las, mediante la aplicación de un campomagnético externo (imanes
o generados por instrumental médico) o internos (implantados qui-
rúrgicamente), hacia los tumores (“
targeting
activo”) (5). El “
targe-
ting
pasivo”, responsable de que las NPs se acumulen en zonas de
tejido tumoral por el fenómeno EPR, permite su aplicación diagnós-
tica, en donde la presencia de compuestos paramagnéticos como
Fe (ya sea en forma de magnetita, Fe
3
O
4
, o de magnemita, Fe
2
O
3
)
puede ser detectada por equipos de Resonancia Magnética Nuclear
(RMN) con alta precisión lo que está permitiendo en muchos casos
realizar un diagnóstico más precoz de tumores, especialmente de
aquellos de muy pequeño tamaño, y por tanto mejorar el pronósti-
co de estos pacientes (6). Por otra parte, el “
targeting
activo” tiene
una aplicación fundamentalmente terapéutica, ya que los campos
magnéticos (ya sean externos e internos) potencian la acumulación
de NPs funcionalizadas con núcleos magnéticos, lo que induce una
mayor concentración de citotóxicos en el tejido tumoral y por tanto
una mayor actividad antineoplásica (7).
Nuestro objetivo en este trabajo es hacer una revisión sobre
los avances más importantes en el uso de NPs funcionalizadas con
núcleos magnéticos en el tratamiento, diagnóstico y teragnosis del
cáncer, destacando las principales experiencias de laboratorio en
modelos
in vitro
e
in vivo
, especialmente aquellas que han tenido
una traducción en la clínica a través del desarrollo de ensayos.
DIAGNÓSTICO, TRATAMIENTO Y TERAGNOSIS CON NANO-
PARTÍCULAS FUNCIONALIZADAS CON NÚCLEOS MAGNÉTICOS
Diagnóstico
Como se ha mencionado anteriormente, las NPs tienden a
localizarse en el tejido tumoral por “
targeting
pasivo” gracias al
efecto EPR. Al tratarse de NPs funcionalizadas con núcleos magné-
ticos, es decir, que están formadas por un núcleo paramagnético
como el hierro, pueden ser detectadas mediante técnicas de RMN,
permitiendo el diagnóstico de tumores de tamaños de hasta 2-3
mm de diámetro, lo que posibilitaría su diagnóstico precoz y por
consiguiente, un mejor pronóstico y supervivencia (Figura 2).
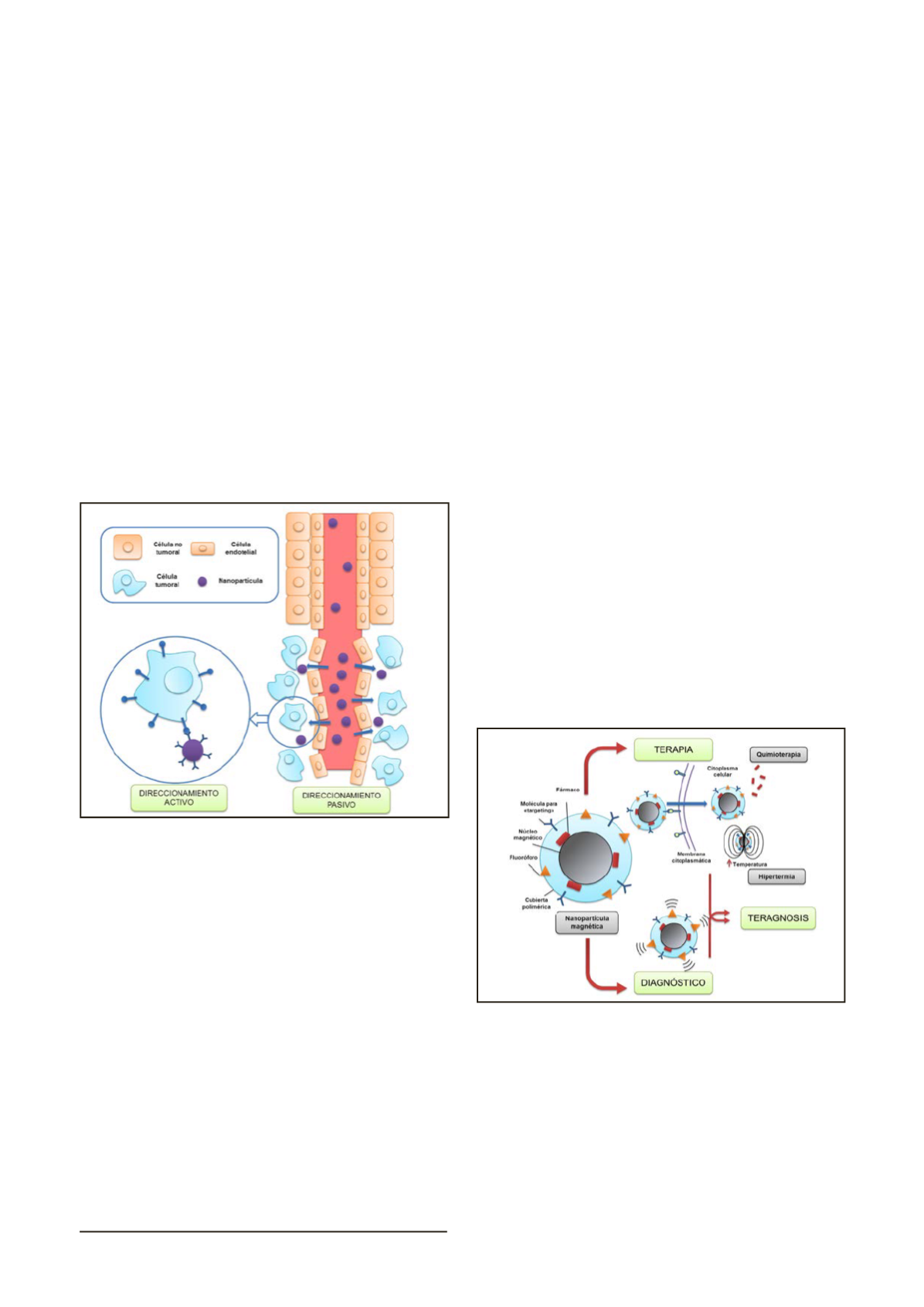
Figura 1. Diferentes tipos de “targeting” de las NPs hacia los
tumores. El “targeting” pasivo se basa en el efecto de permeabilidad
y retención aumentada por el que las NPs se extravasan más
fácilmente de los vasos sanguíneos de los tejidos tumorales (alta
permeabilidad) que de los vasos sanguíneos de los tejidos sanos
(baja permeabilidad). En el “targeting” activo, la superficie de las
NPs son funcionalizadas con anticuerpos u otro tipo de ligando
para que sea internalizada solo por las células diana.
Figura 2. Composición de una NP funcionalizada con núcleos
magnéticos que transporta un fármaco antitumoral y un fluoróforo
y su aplicación en el diagnóstico, tratamiento y teragnosis del
cáncer. El tratamiento se produce tanto por la liberación del fármaco
quimioterápico dentro de la célula tumoral (quimioterapia) como
por la elevación de temperatura que se produce cuando se aplica
un campo magnético sobre la NP que contiene un núcleo metálico
(hipertermia). La presencia de un fluoróforo en la NP funcionalizada
con núcleos magnéticos hace que pueda ser detectable en un tejido
diana, así como su detección mediante técnicas de imagen como
RMN debido al núcleo paramagnético de la NP. La combinación
de ambas, terapia y diagnosis en una misma nanoformulación se
conoce como teragnosis.

















