174
Cristina Garrido Colmenero
Síndrome de DRESS inducido por dronedarona
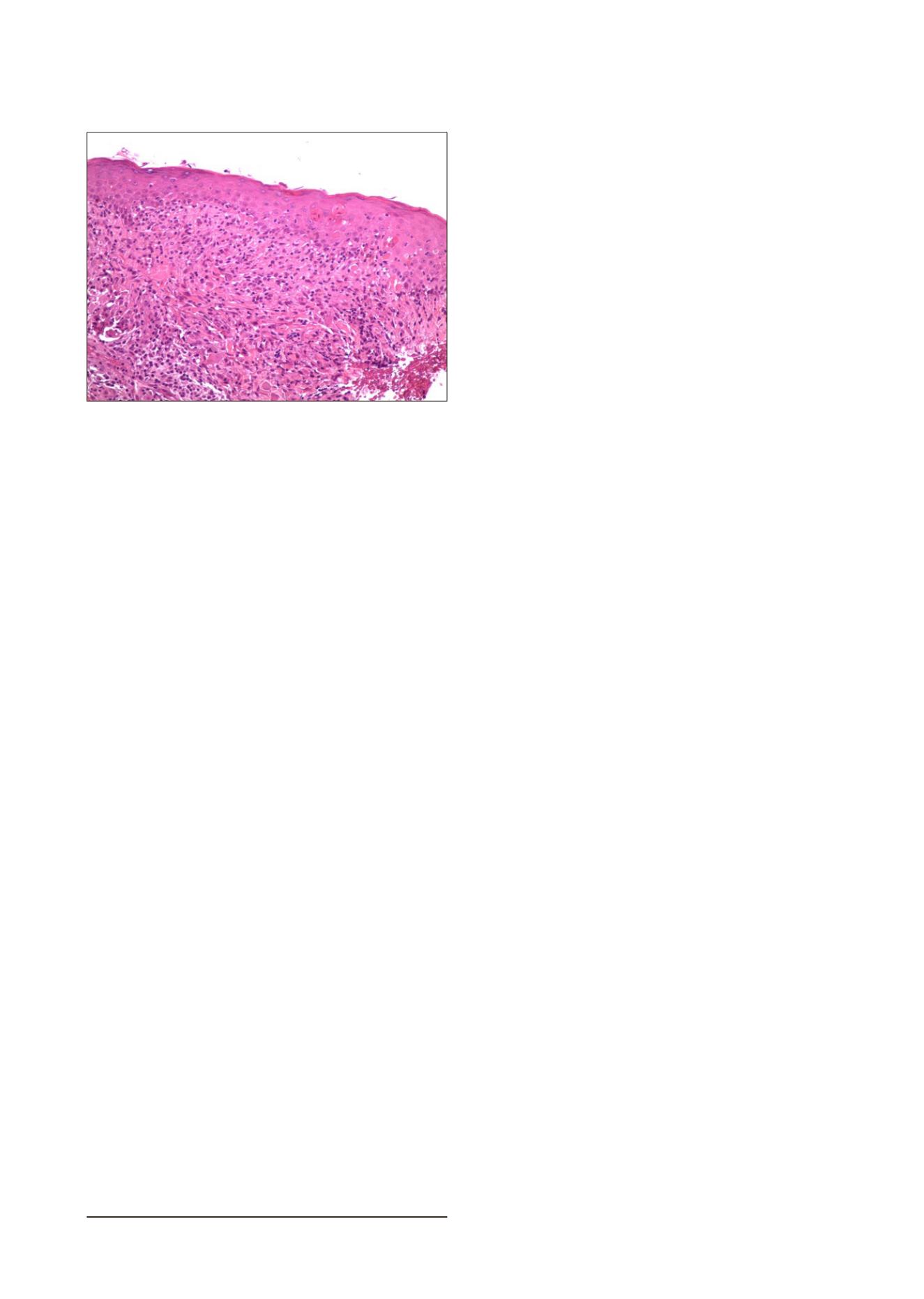
Figura 2. En el estudio histológico podemos observar la epidermis
con ligera espongiosis, abundantes queratinocitos apoptóticos,
ligero edema de dermis superficial e infiltrado linfocitario denso
(Hematoxilina- eosina x 100)
la fiebre y resolviéndose el cuadro dermatológico en aproxima-
damente 10 días.
El síndrome de DRESS presenta manifestaciones cutáneas
en más del 90% de los casos. Por definición, los medicamentos
son la causa del DRESS, habitualmente de 1 a 6 semanas posterior
a la exposición del individuo a éstos. Existe una alta prevalencia
de erupción secundaria a drogas en pacientes con infección por
virus, aunque su mecanismo aún no es bien conocido. Se men-
ciona que las infecciones virales pueden cambiar el metabolismo
de los medicamentos o actuar como señal de alarma activando
la respuesta inmune del huésped. Los virus implicados son virus
herpes tipo 6, Epstein Barr, citomegalovirus, y VIH (4),(5).
La piel es un órgano que contiene isotipos del citocromo
p450, además de ser un órgano inmunológicamente activo por
la presencia de células de Langerhans, lo que la hace susceptible
a reacciones secundarias a medicamentos. Se sugiere además la
implicación de mecanismos de hipersensibilidad celular o de tipo
IV mediada por linfocitos T (6).
El tratamiento más efectivo del síndrome de DRESS es la
suspensión del fármaco desencadenante, el soporte sistémico
(adecuado suministro de oxígeno, hidratación, compensación he-
modinámica, entre otros), así como el inicio de terapia con cor-
ticoides (13). La dosis recomendada de esteroides varía de 0,5
a 1mg/kg. Este tratamiento mejora rápidamente los síntomas y
los parámetros alterados de laboratorio, pero su impacto a largo
plazo en el curso de la enfermedad no es conocido.
Puede que el efecto beneficioso de los glucocorticoides se
deba a la inhibición de la IL5 en el proceso de acumulación de
eosinófilos, como se ha demostrado en el síndrome hipereosi-
nofílico (7),(8).
Otras posibilidades son: ciclosporina, inmunoglobulina hu-
mana, talidomida, interferón y n-acetilcisteína, que ha sido em-
pleada para la detoxificación de múltiples medicamentos (9).
El test de transformación linfocitaria tiene una sensibilidad
general en el intervalo de 60-70% y un conjunto especificidad de
al menos 85%. Un resultado positivo LTT ayuda para definir el fár-
maco causante en la reacción de hipersensibilidad al fármaco, sin
embargo, como la sensibilidad de la LTT es limitada, un resultado
negativo no puede excluir hipersensibilidad al fármaco (10). Con-
secuentemente, el diagnóstico de fármaco hipersensibilidad debe
basarse en una combinación de la historia y diferentes pruebas,
ya que ninguna de las pruebas disponibles solo tiene sensibilidad
suficientemente bueno.
Ante un paciente que ha introducido recientemente varios
fármacos a la vez se recomienda la realización de la prueba del
parche, que es barata e inocua para el paciente.
En nuestro paciente se obtuvo una evolución favorable con
la suspensión del fármaco implicado más la corticoterapia inme-
diata y las medidas de sostén. Hasta la fecha no hay casos publica-
dos de síndrome de DRESS asociados a dronedarona.
REFERENCIAS
1. Rademarker M.: Drug Hypersensivity Syndrome. The New Zeland
Dermatological Society Incorporated, 2005.
2. Mikko T, Yoko Y, Masaki Y y col.Severe hypersensivity syndrome
due to sulfasalazine associated with reactivation of Human Herpes Virus
6. Arch Dermatol 1998; 134: 1113-1117.
3. Ghislain PD, Roujeau JC. Treatment of severe drug reactions: Ste-
vens-Johnson Syndrome, Toxic Epidermal Necrolysis and Hypersensitivity
syndrome. Dermatology Online Journal 2002; 8 (1): 5
4. Wong GA, Shear NH : Is a drug alone sufficient to cause the drug
hypersensivity syndrome?. Arch Dermatol 2004; 140: 226-30.
5. Yong Chang J, Soo-Chan K.: Anticonvulsivant Hypersensitivity
syndrome associated with Epstein Barr Virus Reaction. Yonsei Med J 2007,
48: (2) 317-320.
6. Shapiro L, Shear N. : Mechanisms of drug reactions: the meta-
bolic track. Sem Cutan Surg 1996; 15:217-27.
7. Weller PF, Bubley GJ.: The idiopathic hypereosinophilic syn-
drome. Blood 1994;83: 2759-79.
8. Redondo P, De Felipe I, De la Pena A. y col.: Drug Induced hy-
persensitivity syndrome and toxic epidermal necrolysis: Treatment with
N- acetylcisteine. Br J Dermatol 1997;136: 645-6
9. Krauss G.: Current Understanding of Delayed Anticonvulsant Hy-
persensitivity Reactions. Epilepsy Currents 2006; 6 (2): 33-37
10. Pichler WJ, Tilch J. The lymphocyte transformation test in the
diagnosis of drug hypersensitivity. Allergy. 2004;59:809-20


