
88
Ana Fernández González
Optimización del cultivo de queratinocitos para el desarrollo de un modelo de piel artificial humana
6. Mantenimiento en cultivo de queratinocitos
Se realiza el seguimiento del cultivo a través de microscopio óp-
tico invertido visualizando la morfología y el estado del cultivo, hasta
que alcance el 80% de confluencia y se realice el pase celular. Durante
el tiempo de mantenimiento, cada 48-72 horas se realiza un cambio
deMQT, se desecha el medio de cultivo del frasco y se añade de nuevo
MQT atemperado a 37ºC. Es posible observar alguna colonia de fibro-
blastos procedente del procesamiento inicial del tejido, que será elimi-
nada aplicando una tripsina rápida de 1-2minutos con Tryple Select 1X
en un volumen de 1 ml por cada 25 cm
2
, posteriormente se neutraliza
con medio de cultivo y se desecha, para de nuevo añadir MQT al fras-
co. El frasco se mantiene en el incubador en condiciones estándar de
cultivo: 37ºC y 5% CO
2
.
7. Pase celular de queratinocitos
Una vez alcanzada una confluencia superior al 80% se realiza
el pase celular. El frasco de cultivo de QT se lava con DPBS para rea-
lizar una tripsinización rápida y así poder eliminar cualquier resto de
feeder
que quede en el frasco. Después de la tripsinización rápida,
se añade TrypLE Select 1X en un volumen de 1 ml por cada 25 cm
2
lavando el frasco, desechándolo y posteriormente se vuelve aplicar
este volumen de TrypLE Select 1X dejándolo actuar de 15-30minutos
en el incubador de CO
2
. Las células despegadas del frasco, se neutra-
lizan con el doble de volumen de MQT. La suspensión se recupera en
un tubo estéril de 50ml, se centrifuga a 500g. Se determina el núme-
ro celular y la viabilidad celular con el método Azul Tripan. El número
de queratinocitos obtenidos se siembra en frascos de cultivo T225, la
superficie de cultivo se encuentra cubierta desde el día anterior con
el
feeder
irradiado. La densidad de siembra de los queratinocitos es
de 5000-10000 células/cm
2
. Trasladamos los frascos al incubador de
CO
2
para el posterior mantenimiento de los QT en cultivo, con cam-
bios de medio cada 48-72 horas.
8. Recuperación final de queratinocitos
A las tres semanas de cultivodeQT se realiza la recuperaciónfinal.
Paraello los frascos T225se lavanconDPBS, se realizauna tripsina rápida
conTrypLESelect1XyposteriormenteseincubaconTrypLESelect1X,en
volumen de 1ml cada 25 cm
2
, dejándolo actuar entre 15-30minutos en
el incubador de CO
2
. Cuando se observa que los queratinocitos se han
despegado del frasco, se realiza una neutralización conMQT al doble de
volumen. La suspensión celular se deposita en un falcon de 50 ml y se
centrifuga a 500g, posteriormente se realiza el contaje total de células y
la viabilidad celular con el método de Azul Tripán.
9. Determinación de las variables de estudio
9.1 Número de células y porcentaje de viabilidad celular
La cuantificación de las suspensiones celulares obtenidas, se rea-
lizó utilizando un hemocitómetro (cámara de Neubauer) y aplicando el
método Azul Tripán. De los pellets de células resuspendidos en un vo-
lumen de medio de cultivo conocido, se tomó una alícuota de 10 µl en
un microtubo eppendorf de 0,5 ml. A continuación se añadió un
volumen conocido de Azul Tripán, se homogeneizó bien la sus-
pensión. Se colocó un cubreobjetos sobre la cámara de Neubauer,
y se cargó 10 µl en la parte superior y 10 µl en la parte inferior.
La observación de la cámara se realizó bajo microscopio óptico
invertido. Para cada muestra se contaron los 8 campos de la cá-
mara, obviando las células que se encontraban en los bordes in-
ternos de cada cuadrante.
Se utilizó el método Azul Tripán para la diferenciación de
células vivas y muertas. Se trata de un colorante que no penetra
en las células viables, que al tener su membrana intacta, se ven
como refringentes, y las células muertas se observan de color azul
porque el colorante entra a través de su membrana dañada.
La solución de Türk se utilizó para la tinción de células mononu-
cleadas, y determinar las células viables en el procesamiento inicial para
la obtención de FH, ADMSC y QT.
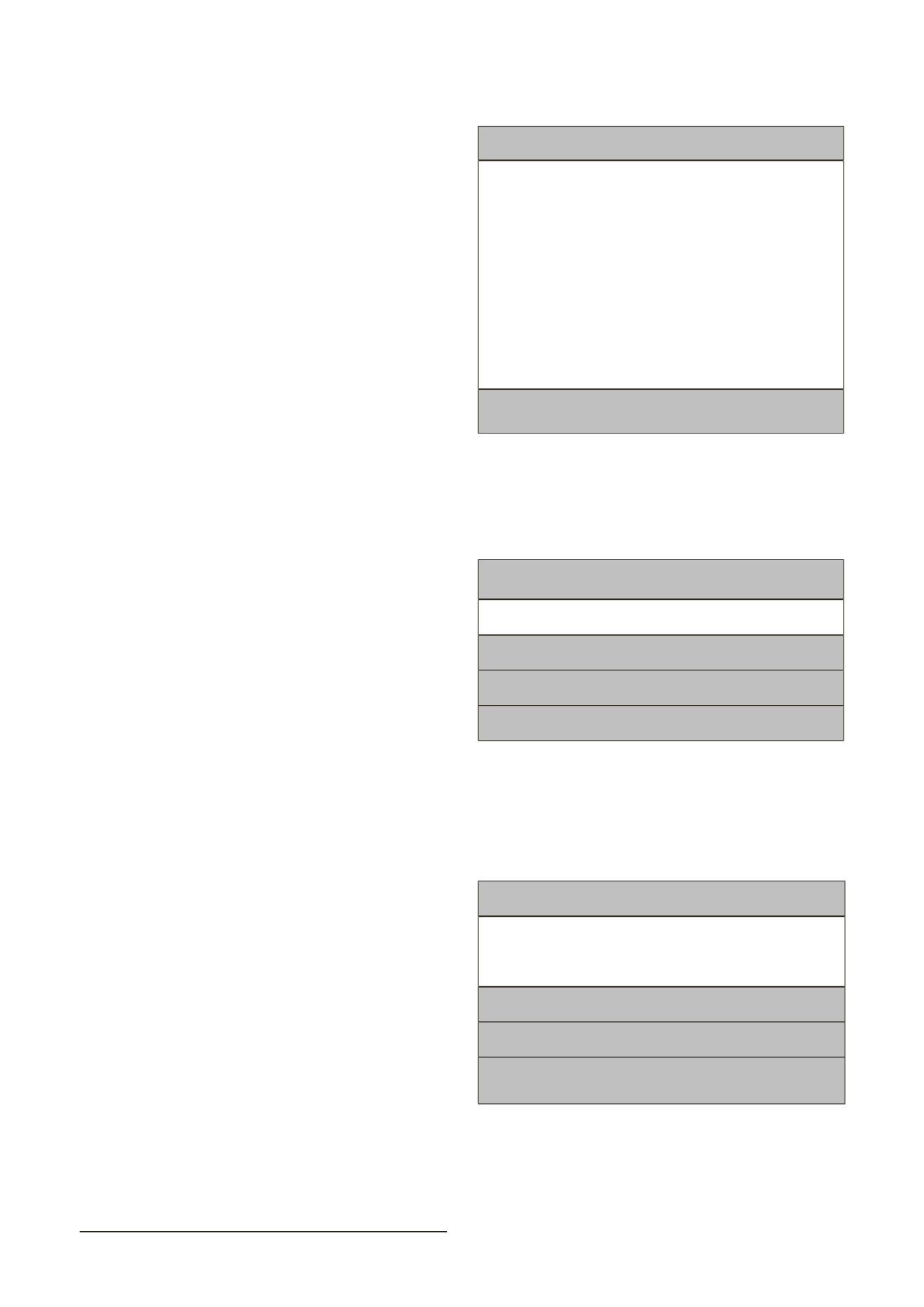
El número total de células viables existentes en la suspensión celu-
lar original fue determinado usando la siguiente formula:
9.2 Tasa de duplicación celular
La variable tasa de expansión celular se estimó en función del
número de células obtenidas en relación al número de células sem-
bradas, determinando el número de veces que la población celular
se incrementa. La fórmula aplicada se resume a continuación:
9.3 Tasa de duplicación celular
En relación a la tasa de expansión celular, se pudo calcular
la tasa de duplicación celular, para evaluar el número de veces
que la población se duplicó en función del número de pases. Los
resultados se expresaron como valores acumulados, aplicando la
siguiente fórmula:
10. Análisis de las variables de estudio
En cada una de las fases del cultivo celular de queratinocitos
se analizaron todas las variables de estudio, a excepción del pro-
N = n/8 x FD x Volumen de resuspensión x 10
4
N = Número de células totales
n = Número de células contadas en toda la cámara
8 = Número de cuadrantes
FD = Factor de dilución (número de veces que la muestra es diluida en
Azul Tripán)
Volumen de resuspensión = Volumen total en el cual el pellet es resus-
pendido
10
4
= Factor de corrección, cálculo en ml, el volumen de muestra es 0,1
µl
Se determinó el porcentaje de viabilidad celular utilizando la misma pre-
paración utilizada para el recuento celular, aplicando la siguiente fórmula:
% Viabilidad Celular = [Nº Células vivas / (Nº células vivas + Nº
células muertas)] x 100
Tasaexpansióncelular=NºCélulasobtenidas/Nºcélulassembradas
De este modo, se obtiene la tasa de expansión celular F1, la tasa de
expansión celular RF y la tasa de expansión celular total:
Tasa expansión celular F1 =Queratinocitos F1 / Queratinocitos F0
Tasa expansión celular RF =Queratinocitos RF / Queratinocitos F1
Tasa expansión celular total =Queratinocitos RF /Queratinocitos F0
Tasaduplicacióncelular=logN/log2
N=Tasadeexpansióncelular=NºCélulasobtenidas/Nºcélulassembradas
Deestemodo,seobtienelatasadeduplicacióncelularF1,latasadeduplica-
cióncelularRFylatasadeduplicacióncelularacumulada:
TasaduplicacióncelularF1=log(QueratinocitosF1/QueratinocitosF0)/log2
TasaduplicacióncelularRF=log(QueratinocitosRF/QueratinocitosF1)/log2
Tasaduplicacióncelularacumulada=TasadeduplicacióncelularF1+Tasade
duplicacióncelularRF

















