
87
Ana Fernández González
Optimización del cultivo de queratinocitos para el desarrollo de un modelo de piel artificial humana
3. Proceso de irradiación
Las células utilizadas como capa alimentadora se irradia-
ron subletalmente.
El proceso de recuperación celular para irradiación se ha
detallado en el apartado anterior. Las células recuperadas se
concentraron a 4.000.000 células/ml y se depositaron en un
tubo estéril de 50 ml sellado con parafilm. El tubo estéril se de-
positó en el interior de un tubo cónico de 500 ml sumergido
completamente en agua, se colocó en una nevera refrigerada
2-8ºC y se transportó al Servicio de Medicina Nuclear del Com-
plejo Hospitalario Universitario de Granada. El tubo estéril de 50
ml que contenía las células se situó en un contenedor metálico
específico relleno de agua en posición vertical a una distancia
de 195 mm de la fuente de radiación. La dosis de radiación fue
50 Gy durante 28 minutos en las líneas 3T3 y FH, salvo la línea
ADMSC que fue irradiada a 50 Gy y 100 Gy en dos pruebas dife-
rentes (Tabla 1). El equipo empleado fue una unidad de irradia-
ción por rayos gamma BIOBEAM 8000 con una fuente de Cs-137
de 2000 Ci.
Transcurrido el tiempo de irradiación, las células se trans-
portaron a la UPCIT en nevera refrigerada 2-8ºC. Se centrifuga-
ron a 800g, para realizar el contaje de células y determinar la
viabilidad celular con el método Azul Tripán, para la posterior
siembra de cada
feeder.
4. Densidad de siembra como
feeder
Las células utilizadas como capa alimentadora previamen-
te irradiadas: fibroblastos 3T3 irradiados (3T3i), fibroblastos
dérmicos humanos irradiados (FHi) y las células madre mesen-
quimales derivadas de tejido adiposo irradiadas (ADMSCi) se
sembraron a diferentes concentraciones de siembra el día pre-
vio a la obtención de Queratinocitos (QT). (Tabla 1)
Las cuatro líneas celulares se sembraron en un frasco T75
(75 cm
2
) previo a la obtención de queratinocitos durante el pro-
cesamiento inicial F0. En el pase celular F1, se sembraron en
frascos T225 (225 cm
2
) pero siempre manteniendo la densidad
de siembra establecida.
Los frascos que contenían la capa alimentadora se mantu-
vieron en condiciones estándar de cultivo hasta el día siguien-
te que se realizó la siembra de los queratinocitos obtenidos
tras el procesamiento inicial del tejido abdominal o durante el
pase celular F1.
5. Procesamiento inicial de piel abdominal: obtención
de queratinocitos (QT) primarios
Los queratinocitos (QT) se obtuvieron a partir de piel ab-
dominal y circuncisiones a través del Biobanco del Sistema Sa-
nitario Público Andaluz y el Servicio de Urología del Complejo
Hospitalario Universitario de Granada, respectivamente; previo
consentimiento informado del paciente en cumplimiento de
los requisitos de donación de células y tejidos humanos (Real
Decreto-ley 9/2014, de 4 de Julio).
Las muestras de piel abdominal de 9 cm
2
de tamaño se
transportaron en DPBS desde el quirófano al laboratorio para
el inicio de su procesamiento. En cabina de flujo laminar, se
mantuvieron en solución de lavado (gentamicina 160 µg/ml,
vancomicina 20 µg/ml, penicilina 600.000 UI, anfotericina B
1,25 µg/ml en DPBS) durante 30 minutos. Posteriormente, con
ayuda de bisturí y pinzas se separó la dermis de la epidermis.
La epidermis se trituró con ayuda de tijeras y se depositó en un
tubo estéril de 50 ml que contenía 10 ml de TrypLE Select 10X
(Gibco) para su digestión enzimática. La digestión se promovió
mediante agitación durante 15 minutos, aplicando cada 5 minu-
tos una agitación manual y así completar un ciclo de digestión.
Este mecanismo se realiza durante 9 ciclos más, en los cuales el
volumen de TrypLE Select 10X aplicado a la muestra de epider-
mis será de 5 ml. Al final de cada ciclo se filtra el contenido del
tubo a través de una malla de 100 µm y se neutraliza la enzima
con el doble de volumen de medio específico para el cultivo de
queratinocitos (MQT): DMEM sin rojo fenol (Sigma), 30% HAM
F-12 (Sigma), 10% suero fetal bovino (Sigma), 1% L-glutamina
200 mM (Sigma), triyodo tironina sódica 20 μg/ml (Sigma), hi-
drocortisona 0,4 μg/ml (Sigma), clorhidrato de adenina 24 μg/
ml (Sigma), factor de crecimiento epidérmico 10 μg/ml (Sigma),
insulina 5 μg/ml (Sigma), gentamicina 96 μg/ml (Normon) y An-
fotericina (Sigma). Después de los 10 ciclos totales, se desecha
el tejido, la suspensión celular se centrifuga a 300g, se desecha
el sobrenadante y se añade MQT para la realización del contaje
celular mediante la solución de Türk y la determinación de la
viabilidad celular mediante el método Azul Tripán. El número
total de células obtenidas se sembró en cada frasco T75 sem-
brado previamente con su
feeder
irradiado el dia anterior.
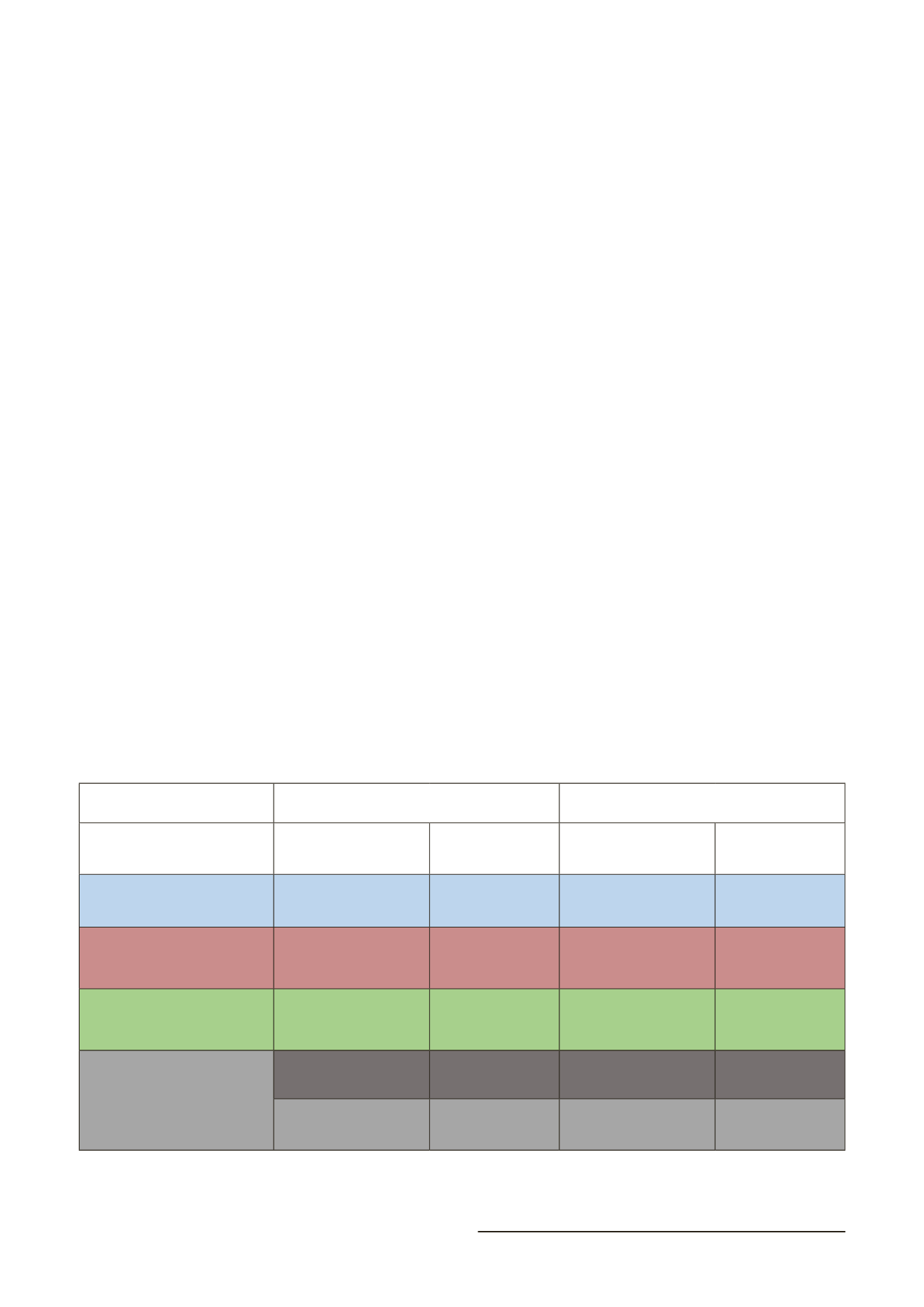
PROCESAMIENTO INICIAL F0
PASE CELULAR F1
Densidad de siembra F0 Dosis de irradiación
F0
Densidad de siembra F1 Dosis de irradiación
F1
Fibroblastos 3T3 (Sigma)
80.000 cél./cm
2
50 Gy
80.000 cél./cm
2
50 Gy
Fibroblastos 3T3 (ATCC)
40.000 cél./cm
2
50 Gy
10.000 cél./cm
2
50 Gy
Fibroblastos dérmicos humanos
(FH)
10.000 cél./cm
2
50 Gy
10.000 cél./cm
2
50 Gy
Células mesenquimales troncales
derivadas de tejido adiposo
10.000 cél./cm
2
100 Gy
10.000 cél./cm
2
100 Gy
10.000 cél./cm
2
50 Gy
10.000 cél./cm
2
50 Gy
Tabla 1. Tipos celulares utilizados como capa alimentadora de queratinocitos. Dosis de irradiación y densidad de siembra en el procesamiento
inicial y en el pase celular.

















